Categoría: Medicamentos
Se retira del mercado la sibutramina
Nota de la Agencia Española del Medicamento
 Suspensión cautelar de comercialización de SIBUTRAMINA (REDUCTIL®):
Suspensión cautelar de comercialización de SIBUTRAMINA (REDUCTIL®):
Como continuación de la nota informativa 2009/13, la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) comunica a los profesionales sanitarios que se ha tomado la decisión de suspender la comercialización de sibutramina, disponible en España con el nombre comercial Reductil®.
Tras la revisión de los resultados preliminares del estudio SCOUT (Sibutramine Cardiovascular OUTcome trial) y los datos disponibles sobre la eficacia de sibutramina, el Comité de Medicamentos de Uso Humano (CHMP) de la Agencia Europea de Medicamentos (EMA) ha concluido que, con la información actualmente disponible, el balance beneficio-riesgo de sibutramina es desfavorable. Como se informó previamente en la nota informativa 2009/13, el estudio SCOUT se diseñó para conocer el impacto de la pérdida de peso obtenida con el tratamiento con sibutramina sobre el riesgo cardiovascular en pacientes con alto riesgo cardiovascular. Este estudio incluyó aproximadamente 10.000 pacientes con una duración de tratamiento de hasta 6 años.
El beneficio a largo plazo observado en estudio SCOUT para sibutramina en términos de pérdida media de peso fue muy modesto en relación a placebo (3,6 kg vs 1,6 kg). Por otra parte, los resultados mostraron un incremento del riesgo cardiovascular de sibutramina (561/4906, 11,4%) en comparación con placebo (490/4898, 10%) en la variable principal (infarto de miocardio, ictus, o parada cardiaca no mortal y muerte de origen cardiovascular) con un incremento de riesgo del 16% (Hazard Ratio 1,161; IC 95% 1,029-1,311), a expensas de un aumento de la incidencia de infarto de miocardio e ictus no mortales. No se observaron diferencias significativas entre sibutramina y placebo en cuanto a mortalidad global.
Aunque la mayoría de los pacientes incluidos en este estudio no serían candidatos al tratamiento con sibutramina en las condiciones de uso autorizadas (fundamentalmente por presentar patología cardiovascular que supone una contraindicación del tratamiento), el CHMP ha considerado que los resultados del estudio SCOUT son
relevantes para el uso del medicamento en la práctica clínica habitual teniendo en cuenta que los pacientes con sobrepeso suelen tener mayor riesgo cardiovascular y que este puede ser difícil de identificar.
En base a estos resultados, se ha concluido que el beneficio esperado para sibutramina no supera los riesgos potenciales, recomendándose por tanto la suspensión de la autorización de comercialización de los medicamentos que contienen sibutramina. Dicha suspensión de comercialización se formalizará con la correspondiente decisión de la Comisión Europea.
Mientras tanto, la AEMPS considera necesario indicar a los profesionales sanitarios lo siguiente:
- Médicos prescriptores: no deberá prescribirse Reductil® a partir del 1 de febrero de 2010, por lo que no deben iniciarse nuevos tratamientos ni continuarse los actualmente en curso.
- Farmacéuticos: no debe dispensarse ninguna prescripción de Reductil® ni elaborar ninguna fórmula magistral con el principio activo sibutramina a partir del 1 de febrero de 2010. En el caso de que un paciente solicite una dispensación de Reductil®, se le debe informar que se ha suspendido la comercialización de dicho medicamento y que debe consultar con su médico para valorar las alternativas disponibles para su caso particular. Las devoluciones al laboratorio comercializador se harán por los cauces habituales.
Se puede consultar la nota pública y documento de preguntas y respuestas de la EMA en su página web: nota de prensa e información para pacientes así como la información para pacientes en español de la agemed
e-David contra Goliat
Efectivamente el pequeño David electrónico, personalizado por un médico de familia radicado en Plasencia, ha podido esta vez, una vez más, con Goliat. Un gigante creado por un laboratorio farmacéutico, vestido por un gabinete de comunicación y arropado con la colaboración cómplice de organizaciones sanitarias, médicos y periodistas. La campaña de Sensibilización de la Importancia del Dolor, ha reproducido una de tantas campañas que se dan últimamente en el panorama sanitario español cuyo objetivo final es la promoción de un determinado medicamento. Siguen un modelo ya clásico, que nace en la imposibilidad de publicidad directa al consumidor, la creatividad exitosa de los nuevos publicistas y el agotamiento de los canales de comunicación directa con el médico.
 Más o menos funciona así: se busca el problema y el presunto objetivo que van desde el dolor a la hidratación, pasando por el cáncer de cérvix o la salud ósea. Se realiza una campaña general destinada a profesionales, políticos, público general o periodistas (o a todos a la vez), en la que figura una asociación, fundación, liga o similar relacionada con el tema – antigua o creada adhoc-. La que en verdad paga, es la industria farmacéutica o el grupo de presión que corresponda. En esta campaña se exalta de forma genérica la importancia del problema mediante libros blancos, experto(s), premios periodísticos y científicos, jornadas, etc. Se incluyen exageraciones del problema, referencias a lo mal que se hace -por supuesto en atención primaria- y se crea la necesidad imperiosa de encontrar una solución. La solución aparece después en forma de medicamento, tecnología diagnóstica, yogurt con bifidus o agua embotellada, en una promoción distinta pero íntimamente relacionada.
Más o menos funciona así: se busca el problema y el presunto objetivo que van desde el dolor a la hidratación, pasando por el cáncer de cérvix o la salud ósea. Se realiza una campaña general destinada a profesionales, políticos, público general o periodistas (o a todos a la vez), en la que figura una asociación, fundación, liga o similar relacionada con el tema – antigua o creada adhoc-. La que en verdad paga, es la industria farmacéutica o el grupo de presión que corresponda. En esta campaña se exalta de forma genérica la importancia del problema mediante libros blancos, experto(s), premios periodísticos y científicos, jornadas, etc. Se incluyen exageraciones del problema, referencias a lo mal que se hace -por supuesto en atención primaria- y se crea la necesidad imperiosa de encontrar una solución. La solución aparece después en forma de medicamento, tecnología diagnóstica, yogurt con bifidus o agua embotellada, en una promoción distinta pero íntimamente relacionada.
Los protagonistas de estas historias denunciadas en este y otros blogs, son tres: la industria, los gabinetes de comunicación y los profesionales. En ese último grupo se incluye médicos expertos con intereses a veces no muy confesables, pero también asociaciones de pacientes “profesionales”, atolondrados médicos y periodistas que recogen el papel de pringaillos difusores del mensaje, y a veces la administración que hace de panoli garante de unos intereses contrarios al bien público. En mi opinión los malos, o los peores, de la película son los profesionales colaboradores interesados pero eso ya es otro asunto.
Pero esta vez la cosa ha sido distinta, gracias a Internet y un médico de familia respondón, un periódico de tirada nacional e influencia- EL PAÍS– ha sacado a la luz este tipo de maniobras y en concreto el entramado de una de estas campañas, que llevaba un tiempo promocionándose en medios profesionales y que se situaba en la fase final de aparición del producto solución. La Plataforma Sin Dolor y la campaña de Sensibilización de la Importancia del Dolor cumple todos los requisitos comentados más arriba -incluido el insulto a la atención primaria- y algunos más (lo del dolor y sus especialistas es digno de estudio)
Bien es verdad que se han utilizado vías de comunicación tan antiguas como las cartas al director y que se ha contado de forma inesperada con la sensibilidad de la defensora del lector especializada en temas sanitarios, pero también que sin Internet y el poder que da a los pequeños nunca se hubiera producido tan desigual batalla y mucho menos se hubiera ganado.
Parafraseándo el lema de la infausta campaña «Cada dolor tiene su historia, EVAlúalo» podriamos decir «Cada campaña relacionada con la salud tiene sus (dos) historias: una confesable y otra no tanto ¡COÑO…celas!
Enhorabuena Enrique.
Sibutramina e incremento riesgo cardiovascular
COMUNICACIÓN SOBRE RIESGOS DE MEDICAMENTOS PARA PROFESIONALES SANITARIOS
Ref: 2009/13 18 de diciembre de 2009
NOTA INFORMATIVA : SIBUTRAMINA E INCREMENTO DE RIESGO CARDIOVASCULAR
La Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) informa a los profesionales sanitarios sobre la revisión del perfil de seguridad de sibutramina, que está llevando a cabo el Comité de Medicamentos de Uso Humano (CHMP) de la Agencia Europea de Medicamentos.
Sibutramina está comercializada en nuestro país con el nombre Reductil®, en cápsulas de 10 y 15 mg. Su uso está indicado como terapia complementaria dentro de un programa integral de control de peso en pacientes con obesidad, o pacientes con sobrepeso que presenten otros factores de riesgo como diabetes tipo 2 o dislipidemia.
En dicha revisión se están analizando los datos obtenidos en el ensayo clínico SCOUT (Sibutramine Cardiovascular OUTcome trial). El objetivo principal de este estudio fue determinar el impacto del tratamiento a largo plazo con sibutramina sobre el riesgo cardiovascular. Dicho estudio ha incluido aproximadamente 10.000 pacientes obsesos o con sobrepeso, con enfermedad cardiovascular y/o diagnóstico de diabetes tipo 2 con al menos un factor de riesgo adicional para enfermedad cardiovascular. Los pacientes fueron asignados aleatoriamente a recibir tratamiento con sibutramina 10 mg/día o placebo durante un período de 5 años.
De acuerdo con las condiciones de uso autorizadas actualmente para el medicamento, el tratamiento con sibutramina estaría contraindicado en la mayoría de los pacientes incluidos en el ensayo clínico. Entre los resultados principales obtenidos en el estudio, se observa un incremento de riesgo de acontecimientos cardiovasculares graves (como infarto de miocardio o ictus) en los pacientes tratados con sibutramina.
Actualmente, se están valorando las implicaciones que estos datos pudieran tener sobre el uso de sibutramina en la práctica clínica habitual, y se espera que dicha evaluación concluya a finales de enero. Mientras tanto, la AEMPS considera necesario emitir las siguientes recomendaciones sobre el uso de sibutramina:
El tratamiento con sibutramina se debe ajustar estrictamente a las condiciones de uso autorizadas
Se recuerda que:
- El uso de sibutramina está contraindicado, entre otros, en pacientes con antecedentes de cardiopatía isquémica, insuficiencia cardiaca congestiva, taquicardia, enfermedad oclusiva arterial periférica, arritmia o enfermedad cerebrovascular (ictus o accidente isquémico transitorio).
- En aquellos pacientes en los que no se obtenga respuesta adecuada en 3 meses (perdida de al menos un 5% de su peso corporal), se deberá suspender el tratamiento.
- El tiempo de tratamiento no deberá ser superior a un año.
- Se puede consultar la nota pública de la Agencia Europea de Medicamentos en su página web
Asimismo, pueden consultar la ficha técnica y el prospecto de este medicamento en la página web de la AEMPS (www.aemps.es)
buscando en internet
El National Prescribing Service ofrece la posibilidad de matricularnos de forma gratuita en un curso online denominado Finding Evidence-Recognising Hype dirigido a médicos de familia y destinado a mejorar las habilidades y confianza en la evaluación de medicamentos. En total, el programa consta de seis módulos. Más información en El rincon de Sisifo
sobre bifosfonatos
nodoyuna
Ana, que junto a Patri forma el afamado duo gestor nodoyuna sigue sin enterarse. Ademas según reza la información del mismo diario especializado del que hemos sacado esta noticia, han puesto a disposición de los profesionales, por medio de la intranet , un extenso informe en PDF de 42 páginas sobre la gestión de la Gripe A en los centros de salud con el pomposo nombre de Plan de preparación y respuesta a la pandemia por el virus de la gripe A/ H1 N1 en atención primaria.

Todavia no lo hemos leído completo, es muy duro tragarse 42 páginas mal redactadas y en jerga gerencial, pero promete y mucho, hay materia para muchas entradas y alguna de ellas será muy divertida.
medicina artesanal
La práctica de la medicina se nutre de muchas tareas controvertidas. No es que consideremos que la medicina deba ser una ciencia exacta, ni siquiera una ciencia. Que lo de cada maestrillo tiene su librillo, sea el pan nuestro de cada día es casi una anécdota comparado con lo que sucede en bajo el escudo del llamado arte de la medicina cuando se ponen a prescribir medicamentos. Lo de las indicaciones aprobadas en la ficha técnica de los medicamentos esta tan lejano de los médicos prescriptores, como el Atleti del primer puesto en la liga. Pero si solo fuera eso, nos daríamos con un canto en los dientes. Lo peor es cuando encontramos costumbres terapéuticas en franca contradicción con lo indicado técnica y legalmente.
Pongamos por ejemplo las afecciones del piel por ser los dermatólogos especialmente cocinicas. Si se repasa las actualizaciones, monografías, libros y artículos nacionales y extranjeros sobre el tratamiento de la alopecia areata encuentra de forma constante y repetida (a veces sospechosamente repetida ) la recomendación de tratar este problema con corticoides intralesionales (entre otras opciones ).
Prácticamente todos recomienda el uso de acetónido de triamcinolona como corticoide de elección para la inyección intradérmica. En España el único medicamento que tiene triamcinolona en esta forma galénica es el famoso Trigon depot. Pues bien, si uno va a la ficha técnica del producto encuentra:
Lo cual sorprende, pero ellos erre que erre e incluso se atreven a filmarlo. Otro ejemplo siguiendo con la piel y con la alopecia. La S ociedad de ME dice:
y la ficha técnica dice:

por si no teniamos bastante con la ceja
Tras Dr. que quiero dejar de fumar, que se me cae el pelo, no se me levanta, y ahora que me voy antes de tiempo. La pregunta de la temporada en las consultas de atención primaria, va a ser (aparte de Dr. ¿ No tendré la LGE –La Gripe Esa-)
¡Tachin,, Tachin! Doctor, que no me crecen las pestañas
LATISSE ® solución (Bimatoprost- con receta-) para el tratamiento hipotricosis pestañil. Se utiliza para fomentar el crecimiento de las pestañas, haciéndolas más largas, espesas y oscuras. Por si teines tentación de recetarlo puees leer antes el comentario de Boing Boing
uso (ir)racional del medicamento
el qui-kit
por Manuel Merino No me resisto a copiarlo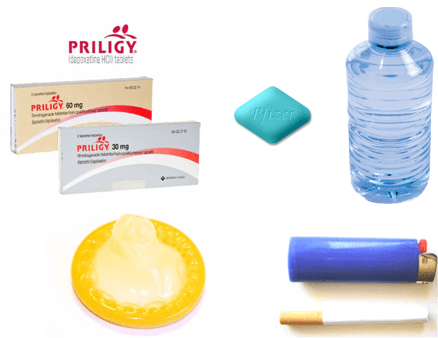
Dícese del equipo mínimo varonil para la cosa de sexo seguro (seguro que hay sexo… vamos, ¡fijo!) a ciertas edades en las que la naturaleza ya nos tiene destinadas otro tipo de actividades menos gimnásticas… pero si hay que cumplir, pues se cumple.
El QUI-KIT, que se distribuye en packs de 2 y 10 bolsas mono-quiqui, contiene 6 unidades o gadgets cuya utilización debe ser secuencial, atendiendo a las siguientes fases:
1.- Fase de preparación: 1 comp. de PRILIGY®* + 1 comp. de VIAGRA® + botellín de agua
2.- Fase de consumación: 1 preservativo no saborizado
3.- Fase de vueltasuser: 1 pitillo + minimechero
QUI-KIT saldrá a la venta directa en bingos y hogares del jubilado, así como por medio de máquinas expendedoras en áreas de petanca y otras zonas de recreo. Se prevé también la distribución a través del clásico estraperlo para los varones no pensionistas