Etiquetado: estatinas
Musculo y estatinas
El estudio StatinWISE, publicado a principios de 2021 en BMJ, sorprende por tres razones: la primera por su metodología, ya que emplea un diseño poco conocido como el ensayo de n igual a 1 a; la segunda, porque pone de relieve un problema frecuente y tercero porque da resultados que, sin duda, resultan polémicos. El artículo en cuestión es un ensayo n = 1 (más bien una serie de ensayos n = 1) multicéntrico, aleatorizado y controlado con 200 pacientes que habían interrumpido poco antes el tratamiento con estatinas o estaban considerando interrumpirlo, debido a síntomas musculares. Los participantes fueron distribuidos de forma aleatoria a una secuencia de seis períodos de tratamiento (de 2 meses cada uno) doble ciego, con 20 mg de atorvastatina una vez al día o placebo con doble ciego. El análisis primario comparó los síntomas musculares evaluados por los participantes en una escala visual analógica (0-10) durante los períodos de estatina o placebo. Los participantes incluidos en el análisis no mostraron diferencia en las puntuaciones de los síntomas musculares en los períodos de estatinas y los de placebo (diferencia de medias de estatinas menos placebo –0,11, intervalo de confianza del 95%: de –0,36 a 0,14; p = 0,40). En cuanto a los resultados secundarios: un 88% dijeron, a los 3 meses de finalizar el último tratamiento, que el ensayo había sido útil; dos tercios de los participantes que completaron el ensayo informaron que reiniciarían el tratamiento a largo plazo con estatinas que habían seguido con anterioridad. La suspensión de la medicación debido a síntomas musculares no tolerables fue del 9% durante el período de estatinas y del 7% durante el período de placebo.
Los resultados de este estudio es probable que sean válidos, pero ponen muy en cuestión una creencia arraigada en Atención Primaria y que, a tenor de los resultados, parece que ha sido exagerada. Cuando un paciente consulta por síntomas musculares frecuentes, como dolor, debilidad, sensibilidad, rigidez o calambres, es un clásico en las consultas, achacarlos a la toma de estatinas. Se ha sumado a la lista de efectos adversos comunes de medicamentos muy utilizados que cualquier profesional tiene en mente. Sin embargo, aunque la percepción por parte de pacientes y profesionales sea esa, parece que los dolores musculares por estatinas no tienen la entidad, ni la frecuencia que, por ejemplo, las cefaleas y edemas maleolares de los antagonistas del calcio, o la tos por inhibidores de la enzima conversora de angiotensina. Además, los resultados sugieren que muchos de estos síntomas serían atribuibles al efecto nocebo. Detener el tratamiento con estatinas debido a estos síntomas musculares inespecíficos no graves, puede tener algún beneficio, como es el caso de una indicación terapéutica no adecuada, tan frecuente con estos fármacos, pero no deja de ser una treta, no muy elegante. Además, puede ocasionar un perjuicio si, como sucedió en el estudio, alrededor del 70% de los participantes tenían enfermedad cardiovascular conocida que requería tratamiento para la prevención del riesgo cardiovascular.
a El ensayo clínico de N igual a 1 es un tipo de ensayo en el que toda la población se limita a un paciente que recibe consecutivamente y por períodos de tiempo el fármaco o intervención y el comparador o placebo, el orden de administración de los tratamientos comparados se determina de manera aleatoria; podríamos decir que el paciente hace su propio control en períodos consecutivos.
Publicado en Bravo Toledo R. Leyendas en la consulta de una médica de familia. AMF 2021; 17(8); 489-490
Estatinas y mayores: pues por ahora, va a ser que no.
Cuando María leyó el tuit sobre el articulo enseguida se lo hizo saber a Luis. Ella conocía la renuencia de su compañero a iniciar y mantener tratamiento con estatinas a los ancianos sin enfermedad cardiovascular previa, por mucho que alguien, un día aciago, les pidiera y encontrará elevado, el colesterol. A María, siempre le había parecido un compañero algo excéntrico; que puede ser más extraño que un médico al que no le gusten los medicamentos y que dude de medidas preventivas de reconocido prestigio y eficacia. Por eso, aunque muchas veces le daba la razón, María no dudo en comentarlo: “Pues parece que hay un meta-análisis que dice que a los mayores también hay que darles estatinas” dijo con cierto retintín. “No lo he leído” le contesto Luis, así que lo mirare y te cuento
Las expectativas no eran nada halagüeñas para la posición de Luis, según pudo leer en Twiter: “Las estatinas producen reducciones significativas en eventos cardiovasculares importantes cualquiera que sea (independientemente de) la edad” incluso había quien se atrevía a elevar la apuesta y exclamaba “Las estatinas reducen la mortalidad y complicaciones CV en todas las edades”
Así que armado de lápiz, borra y sobre todo de sano escepticismo, se puso a leer críticamente el artículo de marras. Era una revisión sistemática con meta-análisis de datos individuales publicada dos meses antes en la revista Lancet.
Tras la lectura del resumen, la cosa fue tomando otro cariz, la rotundidad de las conclusiones se moderaba en el último párrafo:
El tratamiento con estatinas produce reducciones significativas en los eventos vasculares mayores independientemente de la edad, pero hay menos evidencia directa de beneficio entre los pacientes mayores de 75 años que aún no tienen enfermedad vascular oclusiva. Esta limitación ahora está siendo abordada por ensayos adicionales.
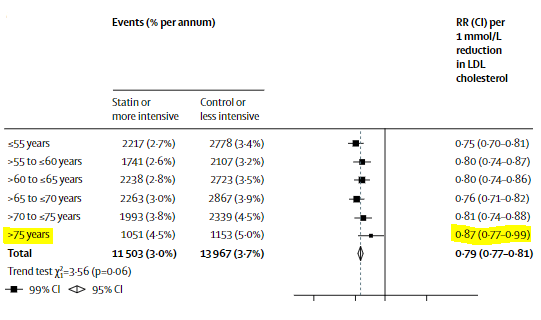 Siguio leyendo y llego a la primera figura donde vio que la razón de tasas de incidencia de la variable eventos vasculares importantes (una variable compuesta por eventos coronarios mayores, revascularización coronaria e ictus) por reducción de 1 mmol / L en el colesterol LDL en pacientes mayores de 75 año, era igual a 0.87 (0.77-0.99 IC del 99%). Cuando el efecto de esta variable se dividía en grupos: con o sin enfermedad cardiovascular previa, la rate ratio pasaba a 0.85 (0.77-0.98 CI 99%) y 0.92 (0.73-1.16 CI 99%) respectivamente.
Siguio leyendo y llego a la primera figura donde vio que la razón de tasas de incidencia de la variable eventos vasculares importantes (una variable compuesta por eventos coronarios mayores, revascularización coronaria e ictus) por reducción de 1 mmol / L en el colesterol LDL en pacientes mayores de 75 año, era igual a 0.87 (0.77-0.99 IC del 99%). Cuando el efecto de esta variable se dividía en grupos: con o sin enfermedad cardiovascular previa, la rate ratio pasaba a 0.85 (0.77-0.98 CI 99%) y 0.92 (0.73-1.16 CI 99%) respectivamente.
¿Que significaban estos datos?
En primer lugar, que el “tamaño” de la reducción del número de eventos era más bien moderado tirando a bajo, y que en el caso de los mayores de 75 años sin enfermedad cardiovascular, la reduccion no es significativa.
Se podía entender mejor, si estas diferencias se expresan en forma de medidas absolutas (diferentes del Rate Ratio que se utilizabs en el artículo), por ejemplo, índices como el NNT (1/ reducción absoluta del riesgo).
Como vemos en la tabla, la reducciones del riesgo muestran diferencias pequeñas, mientras que los NNT son bastante altos. En los mayores de 75 años sin enfermedad vascular, las estatinas no parecen reducir los eventos vasculares principales: NNT 446 (NNH 223 a NNT 132), tampoco se observa en variables de muerte cardiovascular o muerte por cualquier causa.
“Me temo María, que por ahora voy a seguir igual, seguiré intentando que mis pacientes mayores reciban la menor cantidad de estatinas posible. Un abrazo Luis”. Este fue el breve mensaje de wasap que Luis le dejo a su colega, incapaz de esperar al día siguiente para decírselo en persona.
tu colesterol a menos 200
interacciones o cuando el conocimiento importa
Mientras la Comunidad de Madrid-versión Sanidad- sigue muy ocupada en dotar a la Historia Clínica Electrónica (HCE) de un inútil videojuego de pirámides y estratificaciones, se olvida (y ya es demasiado tiempo) de cumplir un aspecto, al que incluso le obliga la ley. No es otro que la implantación de un sistema informatizado de ayuda a la toma de decisiones y en concreto de ayuda a la prescripción. Los usuarios de APedalesMadrid (sobrenombre con el que se conoce el chusco programa de HCE de la Comunidad de Madrid) carecen de una información actualizada para realizar adecuadamente su trabajo.
Afortunadamente la iniciativa privada ofrece soluciones y basta una conexión a Internet para acceder a excelentes recursos como los que ofrece IDoctus (otro día haremos un critica extensa de esta aplicación). Gracias a IDoctus he conocido esta importante interacción que copio a continuación para los que todavía no tiene acceso, aunque deberías registrarte ¡ya!
Este es un servicio proporcionado por iDoctus basado en la base de datos farmacológica del Consejo General de Colegios Oficiales Farmacéuticos (CGCOF) para usuarios del territorio español.
Efecto: La administración conjunta de colchicina con una estatina podría dar lugar a una adición de sus efectos miotóxicos, con mayor incidencia de rabdomiólisis.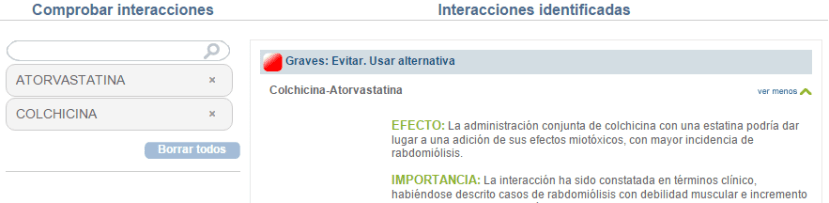
Importancia: La interacción ha sido constatada en términos clínico, habiéndose descrito casos de rabdomiólisis con debilidad muscular e incremento de la creatinina y de la creatín-fosfoquinasa al asociar colchicina con una estatina. En la mayoría de los casos, los pacientes en los que se produjo la rabdomiólisis presentaban además distintos grados de insuficiencia renal, aunque no se puede descartar que esta reacción adversa no se produzca en pacientes con funcionalidad renal normal, ya que tanto la colchicina como las estatinas son conocidos fármacos miotóxicos. Ya que la rabdomiólisis es una reacción adversa muy grave, se recomienda evitar la asociación en la medida de lo posible. Si esto no fuera posible, se deben extremar las precauciones, y realizar un control clínico del paciente, prestando especial atención a los niveles de creatín-fosfoquinasa, así como a la aparición de dolor muscular, cansancio o debilidad.
Mecanismo: Desconocido. Se ha descrito miopatía tanto con la administración de estatinas como colchicina de forma aislada y, por consiguiente, sus efectos pueden ser aditivos. Determinadas pruebas sugieren que también podría intervenir una interacción farmacocinética relacionada con la isoenzima CYP3A4 del citocromo P450, que interviene en el metabolismo tanto de determinadas estatinas (lovastatina, atorvastatina y simvastatina) como en el de colchicina, por lo que tras su administración conjunta se podría incrementar el riesgo. Sin embargo, también se han registrado los síntomas en algunos casos en los que se administró una estatina que no es metabolizada por el isoenzima 3A4 del citocromo P450, como fluvastatina y pravastatina, por lo que se ha propuesto que también podría intervenir una miotoxicidad aditiva.
Evidencias: 1. Un paciente de 45 años, con síndrome nefrótico y amiloidosis, en tratamiento durante dos años con colchicina (1,5 mg/día) acudió al hospital con disnea, astenia y depresión mental. Un mes antes el paciente había iniciado un tratamiento con atorvastatina (10 mg/día), experimentando a las dos semanas dolor muscular. Sus niveles de creatinina y creatín-fosfoquinasa se vieron drásticamente elevados.
2. Se describe un caso de rabdomiólisis en un paciente tratado con fluvastatina y colchicina.
3. Se describe un caso clínico de posible interacción en una paciente de 65 años que experimentó miopatía aguda a los 20 días de añadir colchicina (1,5 mg/día) a su tratamiento con pravastatina. La paciente presentó debilidad muscular. Tras suspender la colchicina, la debilidad mejoró y los niveles enzimáticos volvieron a la normalidad. A los 5 días se reinició la colchicina a dosis de 1,0 mg/día, sin apreciarse reacciones adversas.
4. Se describe un caso clínico en un paciente con insuficiencia renal crónica que experimentó debilidad muscular aguda a las dos semanas de haber comenzado a recibir colchicina, tras 2 años de tratamiento con simvastatina. Tras las pruebas realizadas se determinó que el paciente experimentó rabdomiólisis que se solucionó tras la retirada de ambos fármacos.
5. Se recoge otro caso de rabdomiólisis en un paciente con insuficiencia renal tratado con colchicina y simvastatina.
Referencias:
1. Tufan A, Dede DS, Cavus S et al. Rhabdomyolysis in a patient treated with colchicine and atorvastatin. Ann Pharmacother. 2006; 40(7-8): 1466-9.
2. Atasoyu EM, Evrenkaya TR, Solmazgul E. Possible colchicine rhabdomyolysis in a fluvastatin-treated patient. Ann Pharmacother. 2005; 39(7-8): 1368-9.
3. Alayli G, Cengiz K, Canturk F et al. Acute myopathy in a patient with concomitant use of pravastatin and colchicine. Ann Pharmacother. 2005; 39(7-8): 1358-61.
4. Hsu WC, Chen WH, Chang MT. Colchicine-induced acute myopathy in a patient with concomitant use of simvastatin. Clin Neuropharmacol. 2002; 25(5): 266-8.
5. Baker SK, Goodwin S, Sur M et al. Cytoskeletal myotoxicity from simvastatin and colchicine. Muscle Nerve. 2004; 30(6): 799-802.
¿Más de mil millones de personas tomando estatinas?
 La ACC y la AHA están entre las organizaciones más experimentadas en el desarrollo de guías de práctica clínica. Sus procedimientos son meticulosos, incluyendo transparencia en la comunicación de los conflictos de interés. El trabajo detrás del desarrollo de las guías fue monumental. Las referencias a los ensayos clínicos aleatorizados y revisiones sistemáticas eran continuas (la palabra «evidencia» aparece 346 veces en el informe sobre evaluación del riesgo cardiovascular y 522 veces en el informe sobre el tratamiento). Los panelistas estaban altamente cualificados. Las estatinas se habían evaluado en numerosos ensayos clínicos aleatorizados. Las guías se centraron en resultados clínicos robustos, tales como infarto de miocardio e ictus. Se hicieron advertencias que fueron explicitamente abordadas en documentos que ocuparon cientos de páginas. Sin embargo, esta conjunción de datos y opinión llevaría al uso masivo de estatinas a nivel poblaciones; una «estatinización». No sabemos si esto sería uno de los grandes aciertos o uno de los peores desastres de la historia médica.
La ACC y la AHA están entre las organizaciones más experimentadas en el desarrollo de guías de práctica clínica. Sus procedimientos son meticulosos, incluyendo transparencia en la comunicación de los conflictos de interés. El trabajo detrás del desarrollo de las guías fue monumental. Las referencias a los ensayos clínicos aleatorizados y revisiones sistemáticas eran continuas (la palabra «evidencia» aparece 346 veces en el informe sobre evaluación del riesgo cardiovascular y 522 veces en el informe sobre el tratamiento). Los panelistas estaban altamente cualificados. Las estatinas se habían evaluado en numerosos ensayos clínicos aleatorizados. Las guías se centraron en resultados clínicos robustos, tales como infarto de miocardio e ictus. Se hicieron advertencias que fueron explicitamente abordadas en documentos que ocuparon cientos de páginas. Sin embargo, esta conjunción de datos y opinión llevaría al uso masivo de estatinas a nivel poblaciones; una «estatinización». No sabemos si esto sería uno de los grandes aciertos o uno de los peores desastres de la historia médica.
por defecto
Al igual que algunas de las intervenciones que se efectúan en la práctica diaria no están basadas en la evidencia, y que el exceso de medicalización y medicamentos es cada vez más frecuente, lo contrario también es cierto. Es decir, muchas recomendaciones de reconocida eficacia no llegan a los pacientes y a veces los que se que se beneficiarían de la toma de un determinado medicamento no lo reciben, o al menos no de la forma adecuada.
Las causas de esta falta de consistencia entre lo que se debería hacer y lo que se hace son varias, y muchas de ellas poco conocidas. El conocimiento que guía la práctica no es tan científico (como a priori suponemos) y un cóctel de mitos, modas, manías, miedos e inercias es, a veces, el determinante más importante para la toma de decisiones.
 Así, por ejemplo, la seguridad y la eficacia de las estatinas ha sido ampliamente demostrada para determinadas indicaciones por ensayos clínicos de gran tamaño, pero en la práctica clínica la utilización de estos medicamentos a veces no están correcta. Según los autores de un artículo publicado en el American Journal of the Medical Sciences una de las causas de este mal uso podría ser debida a la preocupación por la hepatotoxicidad de las estatinas entre los médicos de Atención Primaria (AP). Este miedo conduciría a una infraprescripción, especialmente en pacientes con valores elevados de transaminasas hepáticas o enfermedad hepática subyacente.
Así, por ejemplo, la seguridad y la eficacia de las estatinas ha sido ampliamente demostrada para determinadas indicaciones por ensayos clínicos de gran tamaño, pero en la práctica clínica la utilización de estos medicamentos a veces no están correcta. Según los autores de un artículo publicado en el American Journal of the Medical Sciences una de las causas de este mal uso podría ser debida a la preocupación por la hepatotoxicidad de las estatinas entre los médicos de Atención Primaria (AP). Este miedo conduciría a una infraprescripción, especialmente en pacientes con valores elevados de transaminasas hepáticas o enfermedad hepática subyacente.
Para comprobar su hipótesis, realizaron una encuesta a más de 900 médicos de AP de centros académicos en Estados Unidos. La encuesta consistió en preguntas sobre el uso de estatinas en tres determinadas situaciones clínicas figuradas y que correspondía a pacientes con valores altos de LDL y diferente grado de afectación hepática (valores de las transaminasas hepáticas desconocidos, valores elevados y enfermedad hepática subyacente). Más de un tercio de los encuestados tuvo una sensación falsa de riesgo de hepatotoxicidad con estatinas, y esta apreciación se relacionó inversamente con la prescripción de estatinas.
La percepción por parte de médicos de AP de un aumento del riesgo, aunque no esté fundamentada, actúa como una barrera a la hora de prescribir un determinado medicamento. Si a esto se añade que es frecuente encontrarse en la práctica con pacientes que presentan alteraciones de las transaminasas y a la vez riesgo cardiovascular alto, el dilema está servido. Se estaría hurtando a pacientes que se beneficiarían de un tratamiento con estatinas, la posibilidad de recibirlo, y todo por una alteración del hígado en la que el papel de estos fármacos en su mantenimiento o mala evolución es incierto.
En un análisis post-hoc del estudio GREACE, publicado en Lancet se vió que el tratamiento con atorvastatina en pacientes con elevación de las transaminasas se asoció a una reducción de los episodios cardiovasculares superior incluso a la observada en los pacientes con valores de transaminasas normales. Con todas las reservas que supone extraer conclusiones de este tipo de análisis, estos hallazgos nos darían al menos un plus de seguridad que contrarreste el miedo de los médicos a utilizar estatinas en pacientes con hipertransaminasemia.
No es de extrañar que el editorial de Lancet que aparece el mismo número empiece con el provocador titulo de Liver tests are irrelevant when prescribing statins y que en su texto se diga que Statin-induced hepatotoxicity is a myth citando una revisión-comentario del mismo autor publicada en el American Journal of Gastroenterology.
pesadilla

Parece que las estatinas dan pesadillas y no solo a los controladores del gasto farmacéutico, también a los pacientes que las toman.
HMG-CoA-reductase inhibitors and nightmares or abnormal dreaming