Categoría: Prevención
My Melanoma Melodrama
Traducción de My Melanoma Melodrma por John Horgan
Hace poco me diagnosticaron un «melanoma maligno». En esta columna hablaré de lo que significa realmente mi diagnóstico y de lo que pienso hacer al respecto.
Primero, un poco de historia. Hace algún tiempo, me apareció un lunar en la mejilla derecha. Intenté ignorarlo, porque he sostenido que los estadounidenses tenemos demasiado miedo al cáncer. Pero después de que personas cercanas a mí me insistieran para que me revisara el lunar, visité a una dermatóloga, la Dra. M, en otoño de 2022. Me quito el lunar y, días después, una biopsia confirmó su sospecha de que sólo se trataba de queratosis seborreica, un crecimiento benigno de la piel, no de cáncer.
Ese feliz resultado me hizo confiar en la Dra. M. En enero de este año, le pedí que me examinara un grano persistente y a veces sangrante que tenía en el muslo izquierdo. Después de quitar el grano para hacer una biopsia, me preguntó si podía examinar otras manchas sospechosas. Le dije que sí. Encontró algo extraño en mi espalda y me preguntó si podía tomar una muestra para una biopsia. Le dije que sí.
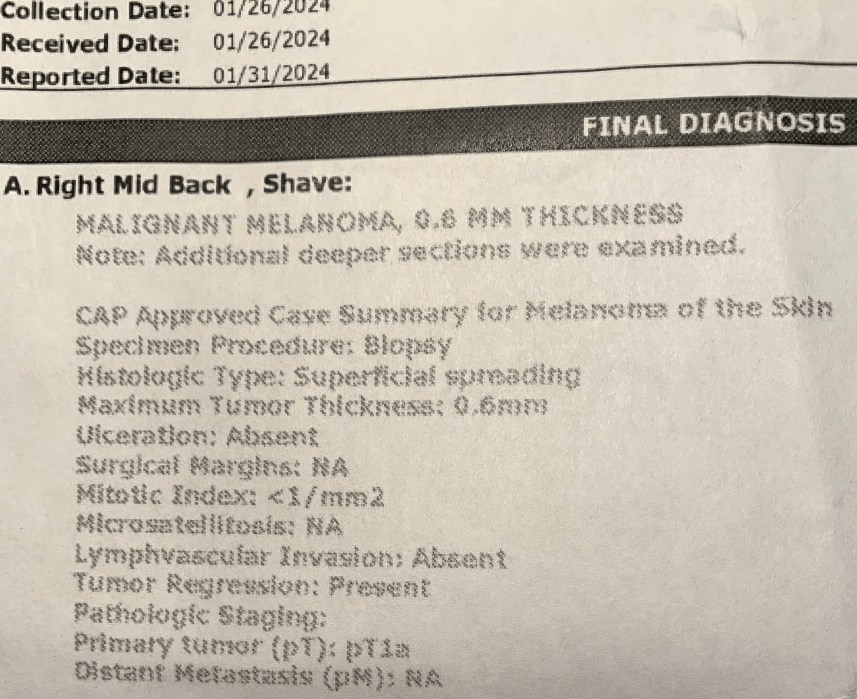
Días después, la Dra. M. me llamó con los resultados de la biopsia. El grano que tenía en el muslo era un carcinoma basocelular. No es gran cosa, los carcinomas basocelulares rara vez o nunca son mortales y bastante tratables; ella podría quemarlo en un procedimiento rápido e indoloro. Pero la mancha de la espalda es un melanoma maligno. Está en estadio pt1a, con un grosor máximo de 0,6 milímetros, o 1/40 de pulgada (véase el informe de la biopsia más arriba).
En este estadio del melanoma, según me dijo la Dra. M., no es necesario comprobar si el cáncer se ha extendido a los ganglios linfáticos ni administrar quimioterapia o radioterapia, pero el tumor debe «extirparse», es decir, extirpar quirúrgicamente el tumor y uno o dos centímetros de piel circundante. Ella no puede hacer esa operación, pero puede recomendarme un cirujano de la red.
¿Y si no hago nada? le pregunté. Aunque ya le había comentado mi extraño e inusual punto de vista sobre la atención oncológica, la Dra. M pareció sorprendida por mi pregunta. El melanoma puede hacer metástasis en otras partes del cuerpo y matarme. La extirpación se puede hacer de forma ambulatoria y tiene una alta tasa de éxito. ¿Por qué no iba a tratarme? Esa fue la respuesta de la Dra. M.
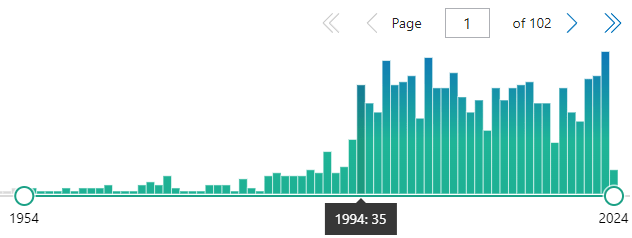
¿Por qué le hice esta pregunta? : ¿y si no hago nada? Entre 1975 y 2017, los diagnósticos de melanoma se multiplicaron por seis, mientras que las tasas de mortalidad se han mantenido más o menos constantes. Este patrón indica que el melanoma se está sobrediagnosticando, lo que significa que los médicos están detectando anomalías que nunca habrían dañado a los pacientes si no se hubieran tratado.
Esa es la conclusión de un estudio del New England Journal of Medicine de 2021 dirigido por H. Gilbert Welch, una autoridad en el sobrediagnóstico del cáncer. Escribí sobre el estudio del NEJM el año pasado en una columna, «Nos asusta demasiado el cáncer de piel».
Desde entonces, han aparecido más pruebas de que «el melanoma se está sobrediagnosticando a un ritmo «alarmante», como dijo la periodista Meryl Davids Landau en National Geographic el mes pasado. Landau cita un estudio del BMJ Evidence-Based Medicine cuyo autor principal es el dermatólogo Adewole Adamson (que también contribuyó al estudio del NEJM de 2021 sobre el melanoma).
Adamson et al estudiaron el melanoma entre los adultos blancos, que corren un riesgo especial de padecerlo. El estudio del BMJ-EBM estimo que, en 2018, «el 49,7% de los melanomas diagnosticados en hombres blancos y el 64,6% en mujeres blancas fueron sobrediagnosticados.» El sobrediagnóstico es particularmente alto entre aquellos diagnosticados con melanoma in situ (también llamado estadio 0), que ocurre solo en la epidermis, la capa más externa de la piel. El estudio del BMJ estima que el 89,4% de los hombres blancos y el 85,4% de las mujeres blancas diagnosticados de melanoma in situ «fueron probablemente sobrediagnosticados».
El estadio inmediatamente superior al melanoma in situ se conoce como melanoma pt1a (o t1a) («pt» significa «tumor primario»). Este es el diagnóstico que recibí. El melanoma T1a se denomina «invasivo» porque el tumor se ha extendido por debajo de la epidermis; pero el tumor tiene menos de 0,8 milímetros de grosor y no muestra signos de metástasis (extensión a otros lugares) ni ulceración (rotura de la piel).
Los melanomas T1a, así como los “in situ”, son responsables de muchos sobrediagnósticos. Esa es la conclusión de un estudio de 2022 en Dermatopathology (citado por Landau) y de otro de 2023 en Pathology. Este último afirma que «una gran fracción de los melanomas que se diagnostican actualmente no causarían la muerte de los pacientes, aunque no se hubieran extirpado.» La cursiva está en el original.
El pronóstico de las personas diagnosticadas de melanoma «localizado», que incluye los cánceres in situ y de tipo t1a, es extremadamente bueno, incluso sospechosamente bueno. La tasa de supervivencia a cinco años es del 99,6%, según el Instituto Nacional del Cáncer.
Esa tasa de supervivencia casi perfecta significa que un melanoma como el mío es «altamente curable», según los promotores del cribado, como la Melanoma Research Alliance. La implicación es que la «detección precoz» y el tratamiento salvan vidas. Pero está claro que muchas personas «curadas» de un melanoma localizado nunca estuvieron en riesgo de morir por la enfermedad y, por tanto, fueron tratadas innecesariamente.
¿Qué debo hacer con la mancha de la espalda? Odio contribuir a la epidemia del sobretratamiento del cáncer. Como ya informé el año pasado, los estadounidenses se someten a pruebas, diagnósticos y tratamientos excesivos de diversos tipos de cáncer a gran escala. Este problema agrava los elevadísimos costes y los malos resultados de la sanidad estadounidense.
Pero si no me opero, seguiré dándole vueltas a esa maldita mancha. El melanoma mata gente: 7.990 en 2023, según el Instituto Nacional del Cáncer. Aunque esa cifra representa sólo el 1,3 por ciento de todas las muertes relacionadas con el cáncer, tengo factores de riesgo de melanoma, como piel clara y ojos azules; miembros de mi familia han sido tratados (con éxito) de melanoma. Por estos motivos, voy a someterme a la extirpación de la mancha de la espalda por un cirujano oncólogo recomendado por la Dra. M.
Si noto otra mancha rara en la piel, probablemente haré que la Dra. M me la revise. Sin embargo, no pienso hacerme revisiones de la piel cada tres o seis meses, que es lo que recomiendan los dermatólogos para los 1.413.976 (en 2020) estadounidenses a los que se les ha diagnosticado un melanoma. Así es como pienso equilibrar mi miedo a morir con mi indignación por el sobrediagnóstico de melanoma.
Más información:
He publicado en este sitio un montón de críticas sobre la atención del cáncer en lugares gratuitos, incluyendo:
La industria del cáncer: Hype Versus Reality
El cribado mamográfico es un experimento fallido
¿Salvan realmente vidas las colonoscopias?
El cáncer de piel nos asusta demasiado
Eche también un vistazo al artículo de Meryl Davids Landau en National Geographic, «El melanoma se diagnostica en exceso a un ritmo ‘alarmante«, que está repleto de enlaces a estudios relevantes, ¡y es demasiado importante para ser de pago!
Por último, para una visión general de las consecuencias de nuestro excesivo miedo al cáncer, consulte el nuevo libro del periodista David Ropeik «Curing Cancerphobia.«
por John Horgan
De los Balcanes al Ministerio de Sanidad
Hace un año nos vimos sorprendidos por la noticia de que el Ministerio de Sanidad financiaba un nuevo medicamento para dejar de fumar. La sorpresa no fue tanto porque se comunicará a la prensa antes que a los profesionales, hecho habitual en todas las administraciones sanitarias, sino porque era un fármaco apenas conocido en nuestro ámbito, a pesar de que como se recogía en la noticia estaba disponible en España algunos años antes. El medicamento era la citisina o citisiniclina (marca comercial Todacitan® al que a finales de año se ha unido Recigarum® y un genérico no comercializado).
La citisina es un alcaloide que actúa como agonista de los receptores nicotínicos ya que tiene una estructura molecular similar a la de la nicotina. Durante la Segunda Guerra Mundial, en los Balcanes, los fumadores utilizaban las hojas de Cytisus laburnum, ricas en citisina, para suplir la carencia de tabaco y pocos años más tarde un laboratorio búlgaro, comercializo el principio activo como tratamiento para dejar de fumar bajo la marca Tabex.
Si uno indaga un poco sobre el fármaco se topa varias peculiaridades: en primer lugar, que el principio activo es de origen vegetal y se puede considerar, por tanto un medicamento “natural” como así se hace en otros países y en Internet. También sorprende que pesar de no ser un fármaco nuevo, los ensayos clínicos publicados son escasos y relativamente recientes en comparación con la antigüedad del fármaco.
Como se relata en las primeras revisiones sistemáticas, las publicaciones iniciales sobre la citisina sufrieron una difusión escasa, dadas las barreras políticas, lingüísticas y, porque no decirlo, por su pobreza metodológica. A partir del comienzo de la primera década del siglo XXI empiezan a aparecer en revistas “occidentales” ensayos clínicos y revisiones sistemáticas que seguían los estándares de realización y publicación
En ese momento se empieza a considerar su utilización en clínica. A pesar de que era un medicamento “sin padrinos industriales”, de países comunistas, por tanto, pobres, y poco estudiado, poco a poco (salvo en España que fue de manera brusca) se ha ido posicionando como tratamiento para la deshabituación tabáquica, oponiendo a la escasez de pruebas de eficacia y efectos adversos, una ventaja tan importante como el precio mucho, más bajo que la vareniclina. Suponemos que será esta y no otra, la razón para su atropellada introducción en el mercado español y la financiación por el ministerio con aportación normal por parte del paciente*. Nada más anunciarse la financiación en nuestro país, se incorporó a protocolos y vías clínicas ya que esta implicaba que el paciente debería estar en un programa de apoyo (individual y/o grupal) de deshabituación tabáquica que estuviera implementado en las diferentes comunidades autónomas.
Una última peculiaridad de este fármaco es la estrambótica posología recomendada, que obliga en veinticinco días a cambiar cinco veces de pauta de tratamiento. Esta posología se estableció en 1960 y ha permanecido hasta nuestros días, si bien su justificación no está clara, ni documentada. La complejidad y la exigencia de esta pauta posológica puede favorecer la falta de cumplimiento del tratamiento y la posibilidad de cometer errores de medicación. Es curioso que el lanzamiento (más intenso en prensa, radio y televisión, que por medios científicos) de la segunda marca: Recigarum® se basa en gran parte en proporcionar un blíster modelo calendario que facilita aparentemente, el difícil cumplimiento de una dosis no demasiado estudiada.
Esta compleja pauta de administración se justifica, al parecer, en la farmacocinética del fármaco y su capacidad para imitar los efectos de la nicotina, reduciendo al mismo tiempo los efectos gratificantes de esta y disminuyendo el ansia de fumar. Sin embargo, como decíamos antes no está suficientemente documentada y cada vez más, se piensa en establecer unas pautas más razonables que la actual.
En este sentido se ha publicado recientemente varios ensayos clínicos aleatorizados con este propósito, entre ellos destaca la serie ORCA, el primero de ellos ORCA-1 se publicó hace dos años, su objetivo era comparar dos dosis de citisiniclina (1,5 mg y 3 mg) frente a placebo, y dos pautas de administración: el ajuste descendente conocido, frente a una pauta de 3 veces al día. Los participantes en el grupo de citisiniclina 3 mg tres veces al día tuvieron la tasa de abstinencia más alta.
El año pasado, se publicó en la revista JAMA, se publica el ORCA- 2 donde se ponen a prueba dos posologías de diferente duración (3 mg tres veces al día durante seis semanas y la misma dosis durante doce semanas) entre sí y frente a placebo. Es un ensayo clínico multicéntrico aleatorizado, ciego y con asignación enmascarada. Como variable de resultado se evalúo la abstinencia de tabaco a partir de las tres semanas de iniciar el tratamiento y hasta las seis y doce semanas según la pauta. También se evalúo esta abstinencia a las 24 semanas como variable secundaria. En ambas pautas los resultados fueron favorables a la citisiniclina con odds ratio de 8 para la pauta de seis semanas y de 6,3 para la de doce, calculándose unos NNT de 5 y de 4 respectivamente. Como limitaciones de estudio: hacer notar que tuvo pérdidas de seguimiento de hasta el 28% y fue realizado con unos restrictivos criterios de inclusión. Aun así, con los resultados se puede considerar la citisiniclina como un medicamento eficaz en la lucha contra el tabaco, como se puede confirmar en la tabla de NNTs comparativa publicada en una “pregunta clínica” publicada recién en AMF.
Pero sobre todo muestra que otras pautas de administración son posibles, con la salvedad de que incluso la pauta de seis semanas implica tomar más del doble de medicamento que la esotérica pauta recomendada hasta ahora.
Notas
* El bupropion (Zyntabac) tiene un coste menor para el paciente que las otras dos opciones y goza además de aportación reducida , con lo cual el paciente solo aporta un máximo de 5,45 euros. La retirada del mercado de la vareniclina (Champix) por contaminación por nitrosaminas y el desabastecimiento de bupropion también han colaborado.
Medicina demasiado impertinente
Mitos sobre el cribado. Cómo realizar el cribado con más criterio
traducido de Thériault G, Reynolds DL, Grad R, et al. Debunking myths about screening: How to screen more judiciously. Can Fam Physician. 2023 Nov; 69(11): 767-771
traducción no autorizada con DeppL por Rafael Bravo Toledo. Texto completo en PDF.
En la mayoría de los casos, el cribado se considera un esfuerzo noble y que merece la pena. La mayoría de los pacientes creen que el cribado no tiene inconvenientes y que sólo puede aportar resultados positivos para la salud. Los médicos sabemos que no es así. El objetivo de este artículo es revisar y explicar algunos de los mitos que rodean al cribado. La evolución de la atención al paciente desde las enfermedades infecciosas agudas a las enfermedades crónicas ha influido en nuestro enfoque del cribado y ha contribuido a estos mitos. Asumimos que podíamos abordar las enfermedades crónicas de la misma manera que habíamos combatido las enfermedades infecciosas; sin embargo, no sólo el tratamiento de las enfermedades crónicas no es tan sencillo, sino que los resultados de las pruebas diagnósticas de las enfermedades crónicas rara vez son tan seguros. Esta incertidumbre se amplifica en el caso de los resultados de las pruebas de cribado.
El cribado parte de la premisa de que una prueba aplicada a una persona o población asintomática y elegible, una vez o a intervalos, puede identificar un precursor tratable de una enfermedad (es decir, prevenir la enfermedad) o identificar una enfermedad tratable en una fase más temprana (es decir, prevenir una morbilidad y mortalidad más graves). Para que el cribado sea eficaz, la identificación debe conducir a tratamientos efectivos que beneficien a los pacientes (es decir, que reduzcan la morbilidad y la mortalidad) con magnitudes de daño aceptables. Sin embargo, a menudo la investigación no proporciona la información esencial para cuantificar tanto los beneficios como los perjuicios del cribado. Los pacientes y los profesionales no pueden evaluar el equilibrio y participar en una toma de decisiones compartida y significativa. Esto alimenta suposiciones y mitos sobre el cribado.
Caso Clínico
Por la mañana, mientras hojea una de sus revistas profesionales en Internet, le intriga saber de una nueva prueba de detección de la demencia que permitiría detectarla años antes de la aparición de los síntomas. Su primera impresión es que podría ser una prueba útil en su consulta. Reflexionando un poco más, se pregunta qué beneficios puede tener la detección precoz de la demencia cuando no existe una terapia específica que pueda cambiar significativamente su curso. También se pregunta cómo podría afectar este diagnóstico a las decisiones vitales de los pacientes que obtienen resultados positivos en el cribado, sobre todo teniendo en cuenta la posibilidad de falsos positivos. Empiezas a cuestionarte las ventajas de la detección precoz de otras enfermedades. De hecho, incluso te preguntas: «¿El cribado salva vidas?».
Mito 1: el cribado no es perjudicial
Algunas pruebas de cribado pueden ser beneficiosas, pero rara vez se habla de los posibles daños. Lo ideal sería que, cuando detectamos más enfermedades, pudiéramos tratarlas y mejorar la evolución del paciente. Desgraciadamente, esto no es cierto para todas las enfermedades que se detectan. Una vez realizado el diagnóstico, no es posible saber si la persona tiene un sobrediagnóstico (es decir, una enfermedad que no se habría manifestado a lo largo de su vida) , una enfermedad cuyo pronóstico no podemos cambiar o una enfermedad cuyo pronóstico podemos mejorar. Muchos piensan que sólo ocurre esto último.
El sobrediagnóstico es una consecuencia inherente a cualquier tipo de cribado. Su aparición, así como otros daños potenciales como los resultados falsos positivos, deben estimarse y discutirse con el paciente junto con los beneficios potenciales para determinar si el cribado es algo en lo que embarcarse o no. La comprensión del paciente y su participación en la decisión son fundamentales. Tomemos como ejemplo a un hombre de 70 años que se encuentra bien. Tras una toma de decisiones compartida, el paciente fue sometido a un cribado de aneurisma aórtico abdominal (AAA). Se descubrió un AAA y el paciente fue intervenido quirúrgicamente. Es posible que este paciente se haya sometido a esta intervención quirúrgica por un AAA que nunca le habría causado síntomas en su vida. De ser así, se trataría de un sobrediagnóstico. Dado que el AAA no habría causado síntomas, el paciente no podría beneficiarse de la intervención y sólo podría resultar potencialmente perjudicado (por ejemplo, por complicaciones quirúrgicas). Incluso las personas con AAA pequeños por debajo del umbral para la intervención pueden verse perjudicadas por la vigilancia periódica a la que se someten. Por otro lado, algunos individuos identificados mediante cribado sí se benefician de una intervención quirúrgica más temprana. Dado que los médicos no podemos predecir el futuro, no podemos saber qué pacientes asintomáticos con «enfermedad» se beneficiarán del cribado y de las intervenciones posteriores. El debate sobre los pros y los contras del cribado debe producirse antes de tomar la decisión de realizarlo.
Mito 1: el cribado no perjudica
Algunas pruebas de cribado pueden ser beneficiosas, pero rara vez se habla de los posibles daños. Lo ideal sería que, cuando detectamos enfermedades, pudiéramos tratarlas y mejorar la evolución del paciente. Desgraciadamente, esto no es cierto para todas las enfermedades detectadas. Una vez realizado el diagnóstico, no es posible saber si la persona tiene un sobrediagnóstico (es decir, una enfermedad que no se habría manifestado a lo largo de su vida)3 , una enfermedad cuyo pronóstico no podemos cambiar o una enfermedad cuyo pronóstico podemos mejorar.
El sobrediagnóstico es una consecuencia inherente a cualquier tipo de cribado. Su aparición, así como otros daños potenciales como los resultados falsos positivos, deben estimarse y discutirse con el paciente junto con los beneficios potenciales para determinar si el cribado es algo en lo que embarcarse o no. La comprensión del paciente y su participación en la decisión son fundamentales. Tomemos como ejemplo a un hombre de 70 años que se encuentra bien. Tras una toma de decisiones compartida, el paciente fue sometido a un cribado de aneurisma aórtico abdominal (AAA). Se descubrió un AAA y el paciente fue intervenido quirúrgicamente. Es posible que este paciente se haya sometido a esta intervención quirúrgica por un AAA que nunca le habría causado síntomas en su vida. De ser así, se trataría de un sobrediagnóstico. Dado que el AAA no habría causado síntomas, el paciente no podría beneficiarse de la intervención y sólo podría resultar potencialmente perjudicado (por ejemplo, por complicaciones quirúrgicas). Incluso las personas con AAA pequeños por debajo del umbral para la intervención pueden verse perjudicadas por la vigilancia periódica a la que se someten. Por otro lado, algunos individuos identificados mediante cribado sí se benefician de una intervención quirúrgica más temprana. Dado que los médicos no podemos predecir el futuro, no podemos saber qué pacientes asintomáticos con «enfermedad» se beneficiarán del cribado y de las intervenciones posteriores. El debate sobre los pros y los contras del cribado debe producirse antes de tomar la decisión de realizarlo.
El debate sobre los pros y los contras del cribado debe producirse antes de tomar la decisión de realizarlo
Otros daños están relacionados con las propias pruebas y con posibles investigaciones o tratamientos posteriores. Los falsos positivos pueden preocupar a los pacientes, sobre todo si son frecuentes. Además de provocar ansiedad en una persona sana por la posibilidad de estar enferma, las investigaciones posteriores de los resultados positivos pueden requerir diagnósticos por imagen y biopsias adicionales que no están exentos de consecuencias. El cribado tiene beneficios potenciales, pero como en cualquier decisión clínica, también deben discutirse los perjuicios y respetarse los valores y preferencias de los pacientes. Por ejemplo, antes de prescribir una estatina en prevención primaria, discutimos con los pacientes los beneficios y los perjuicios de su uso. Lo mismo debería hacerse antes de tomar decisiones sobre el cribado.
Mito 2: la detección precoz produce mejores resultados
Una de las creencias más extendidas es que la detección precoz de la enfermedad siempre se traduce en mejores resultados para los pacientes. La detección precoz es necesaria, pero no suficiente, para que el cribado sea beneficioso. Un aumento del diagnóstico precoz por sí mismo no está directamente relacionado con el beneficio, a menos que pueda demostrarse una disminución de la enfermedad avanzada o de la mortalidad.
Bell y Nijsten han comentado cómo el cribado del melanoma aumentó la detección precoz de la enfermedad sin tener ningún impacto sobre la enfermedad en estadios posteriores. Del mismo modo, la historia del cribado del neuroblastoma en Japón (que comenzó en 1985) es aleccionadora. Este cáncer tiene mejor pronóstico cuando se diagnostica antes del año de edad, por lo que el objetivo del programa era identificar el neuroblastoma antes, cuando el pronóstico es mejor. El cribado aumentó la incidencia del neuroblastoma pero no modificó el número de niños diagnosticados más tarde (después del año de edad) y la mortalidad siguió siendo similar a la de otros países sin programas de cribado. Como en el ejemplo del cribado del melanoma, el cribado descubrió casos antes pero no tuvo beneficios globales. El programa de Japón se interrumpió en 2004.
Otro ejemplo de detección precoz de la enfermedad fue la «epidemia» de cáncer de tiroides en Corea del Sur que siguió al aumento del uso de ecografías tiroideas. Ante el aumento de la tasa de cánceres de tiroides, muchos surcoreanos pensaron que el cribado sería útil. Basándose en las virtudes ensalzadas de la detección precoz, el cribado del cáncer de tiroides mediante ecografías dio lugar a que decenas de miles de pacientes fueran sobrediagnosticados, sin cambios en la mortalidad, a pesar de que casi todos los pacientes fueron tratados, muchos de ellos con secuelas. Sin impacto en los beneficios importantes para el paciente y con un gran aumento de los daños (por ejemplo, medicalización, daños del tratamiento), el cribado más frecuente y la detección de más enfermedad no fueron beneficiosos. Aunque en Canadá no se promovió el cribado de tiroides, se observaron aumentos notables en el uso del diagnóstico por imagen durante la década de 1990 y principios de la de 2000, principalmente en mujeres de mediana edad, de nuevo sin cambios en la mortalidad.
A menudo pensamos que las enfermedades se comportan de forma coherente y son predecibles, como se representa en el modelo tradicional de progresión del cáncer de la figura 1 pero la realidad es más variable, como se muestra en el modelo contemporáneo. Ni siquiera el cáncer es siempre una enfermedad lineal y progresiva, por lo que hay que responder a la pregunta «¿es mejor cuanto antes?» antes de sugerir cualquier cribado. Necesitamos pruebas de que, de hecho, es mejor adelantarse, al menos para algunos individuos, y una idea de la magnitud de los beneficios y los daños.

Figura 1.- Dos modelos de progresión del cáncer: El modelo tradicional (izquierda) postula que todos los cánceres están destinados a seguir una progresión ordenada desde el foco primario a los ganglios linfáticos, pasando por focos metastásicos distantes, hasta causar finalmente la muerte del cáncer. El modelo contemporáneo (derecha) es más complejo y heterogéneo. Algunos cánceres son metastásicos desde su aparición (A), otros nunca metastatizan pero causan la muerte por invasión local (B), mientras que otros siguen el modelo tradicional (C). Otros cánceres no están destinados a causar síntomas porque crecen tan lentamente que los pacientes mueren por otras causas antes de que aparezcan los síntomas (D), dejan de crecer (E) o remiten (F).
Mito 3: una tecnología más nueva produce más beneficios
Cuando las nuevas tecnologías permiten detectar más enfermedades, debemos asegurarnos de que su uso produce un balance global positivo en términos de resultados importantes para el paciente.13 Como ejemplos, podemos pensar en la mejora de las pruebas de imagen o en la adición de más pruebas a las ya existentes, como la tomografía computarizada de mayor resolución. Desde la llegada de esta prueba «mejorada», se ha producido un aumento pronunciado de los diagnósticos de embolia pulmonar, lo que se ha traducido en un aumento de la incidencia sin una disminución sustancial de la mortalidad.14 Este es un claro ejemplo de sobrediagnóstico (a través de hallazgos incidentales, no de cribado). En el cribado, la mamografía digital combinada con la tomosíntesis (enlace del T) mamaria puede detectar más cánceres de mama que la mamografía sola, pero esto no debe considerarse una garantía de mejor salud. Podría ser beneficioso, pero se necesita información sobre la magnitud de los posibles beneficios y daños para informar a nuestras pacientes.
En la tabla 1 se describen las distintas formas en que el cribado puede ampliar el reconocimiento de la enfermedad. Los problemas persistentes son la falta de reconocimiento de los daños potenciales y los beneficios no demostrados del aumento de la incidencia de casos.
| MANERA de ABORDAR LA MANERA de AMPLIAR LA DETECCIÓN de ENFERMEDADES | REFLEXIÓN |
| Amplíe el rango de edad de las pruebas de detección para que comiencen antes o terminen más tarde | La incidencia de la enfermedad puede diferir o la morbilidad y mortalidad competitivas pueden empeorar el balance beneficio-daño. Algunos ejemplos son la controversia sobre la edad para comenzar a detectar el cáncer de mama con mamografías. La información transparente sobre la magnitud de los beneficios y los daños es clave para la toma de decisiones compartida |
| Aumentar la frecuencia de las pruebas de detección | Creencia en el beneficio de un cribado más frecuente para no «pasar por alto» los casos sin tener en cuenta los posibles daños (p. ej., las pruebas anuales de Papanicolaou se consideraron necesarias) |
| Usar pruebas de detección más sensibles | El uso de imágenes más sensibles puede identificar lesiones más pequeñas sin evidencia de beneficio de los ensayos clínicos. Un ejemplo sería si se recomendara la resonancia magnética en lugar de la mamografía para la detección del cáncer de mama en mujeres con un riesgo promedio |
| Ampliar las definiciones de enfermedades | La reducción del umbral de anomalía aumentará la proporción de la población diagnosticada con una afección determinada. Algunos ejemplos son los cambios en los criterios de hipertensión, diabetes y trastorno del espectro autista |
Mito 4: el cribado salva vidas
En muchos programas de cribado, especialmente en el del cáncer, se nos dice que el cribado salva vidas. Desgraciadamente, esto rara vez se ha demostrado, aunque algunos estudios hayan encontrado reducciones en la mortalidad específica de la enfermedad. Por ejemplo, las revisiones sistemáticas del cribado del cáncer de mama han mostrado una pequeña reducción de las muertes atribuidas al cáncer de mama pero no de la mortalidad general. Esto es importante, ya que los mensajes clave a menudo se reducen a «el cribado del cáncer de mama salva vidas», mientras que el mensaje debería ser que por cada 1000 mujeres sometidas a cribado repetidamente a lo largo del tiempo, «el cribado del cáncer de mama puede reducir las muertes por cáncer de mama.» La cifra varía según la edad, pero se sitúa en torno a 1 de cada 1000 mujeres sometidas a cribado entre los 50 y los 60 años.
Demostrar una reducción de la mortalidad por todas las causas es un reto para cualquier prueba, sobre todo para las pruebas de cribado en las que la mayoría de las pacientes tienen un riesgo de muerte muy bajo. Los ensayos controlados aleatorizados tendrían que ser muy amplios o el tamaño del efecto tendría que ser sustancial. Una estrategia consiste en combinar varios ensayos para aumentar la potencia estadística. De este modo, la única prueba de cribado del cáncer que muestra una reducción estadísticamente significativa de la mortalidad por cualquier causa es la sigmoidoscopia flexible para el cáncer colorrectal (riesgo relativo = 0,97; IC del 95%: 0,959 a 0,992; p = 0,004), con una reducción del riesgo absoluto de 3,0 muertes por cada 1.000 personas sometidas a cribado (IC del 95%: 1,0 a 4,0) durante 11,5 años de seguimiento. Dado que el cribado del cáncer de cuello uterino disminuye la incidencia de la enfermedad, es probable que también reduzca la mortalidad.
Dado que el cribado se centra en personas asintomáticas y que los resultados del cribado pueden conducir a la medicalización, es importante para nuestros pacientes (y para nosotros mismos) que comprendamos cuál es el beneficio (por ejemplo, la mortalidad específica de la enfermedad) y su magnitud. Debemos evitar la idea más general de salvar vidas. Confrontar los mitos del cribado con la evidencia es un paso importante para reconocer cómo se puede utilizar el cribado de forma más sensata (Tabla 2).
| MITO | REALIDAD |
| Cuanto antes mejor. | Si bien la detección temprana es clave para el éxito de una prueba de detección, necesitamos más información. La evidencia de los ensayos debe mostrar que la intervención mejora la salud si la enfermedad se detecta antes y que los daños resultantes son aceptables |
| Más es mejor | Detectar más enfermedades no es sinónimo de beneficio. Necesitamos información sobre el equilibrio entre beneficios y daños antes de proceder. El indicador más imparcial del beneficio es la mortalidad por todas las causas, pero este resultado rara vez se logra. Los resultados falsos positivos y el sobrediagnóstico son indicadores importantes de daño |
| Lo más nuevo es mejor | Las pruebas más nuevas tienden a verse a través de una lente positiva. Es posible que detecten más enfermedades, pero el uso de estos nuevos métodos debe someterse a ensayos clínicos para demostrar la magnitud de los beneficios y los daños |
| Las pruebas de detección salvan vidas | Este es el mito más perdurable de todos, pero la realidad es más matizada. Los pacientes deben conocer el impacto final en sus vidas de las pruebas de detección basadas en la mortalidad por todas las causas. La mortalidad específica de la enfermedad puede dar lugar a una percepción más favorable del beneficio. Las estimaciones absolutas de los beneficios (y los daños) deben proporcionarse de forma transparente para una toma de decisiones compartida significativa |
Resolución del caso clínico
Durante la comida, vuelves al artículo online sobre la prueba de cribado de la demencia. En él se afirma que la prueba detectó antes la enfermedad en comparación con la atención habitual, pero no hay información sobre resultados importantes para el paciente (por ejemplo, necesidad de cuidados a largo plazo, calidad de vida, mortalidad) y no se informó de los daños. Te das cuenta de que tus reflexiones habían dado en el clavo; se necesita más investigación para evaluar esta intervención. Decide escribir un comentario a continuación del artículo. Al leer los comentarios anteriores te das cuenta de que no eres el único con dudas sobre la importancia clínica de este descubrimiento
.
Conclusion
While there should be a sufficient burden of disease for screening to potentially be appropriate, an increase in incidence should not be the only reason to suggest more screening. Some screening is aimed at very rare diseases with catastrophic outcomes because effective approaches are available to avert these consequences (eg, metabolic diseases in newborns), but, in general, population-based screening for something exceedingly rare (eg, cervical cancer in women younger than 25) would cause many harms (eg, false positives) with very few, if any, benefits. Diseases may increase in incidence because of changing epidemiology (eg, tobacco smoking, obesity, diabetes). If this is suspected, efforts should be made to determine whether systematically addressing these risk factors would be more effective than screening.
In 1968 Wilson and Jungner brought attention to screening by identifying 10 principles to guide its use.22 With the knowledge we have gained since then, we realize that what we had thought was relatively straightforward is much more complicated.23
Conclusión
Aunque debe existir una carga suficiente de enfermedad para que el cribado sea potencialmente apropiado, un aumento de la incidencia no debe ser la única razón para sugerir más cribados. Algunos cribados se dirigen a enfermedades muy raras que tienen resultados catastróficos en los que se dispone de enfoques eficaces para evitar estas consecuencias (p. ej., enfermedades metabólicas en recién nacidos), pero, en general, el cribado poblacional de algo extremadamente raro (p. ej., cáncer de cuello de útero en mujeres menores de 25 años) causaría muchos daños (p. ej., falsos positivos) con muy pocos beneficios, si es que los hay. La incidencia de enfermedades puede aumentar debido a cambios epidemiológicos (por ejemplo, tabaquismo, obesidad, diabetes). Si se sospecha esto, se debe intentar determinar si abordar sistemáticamente estos factores de riesgo sería más eficaz que el cribado.
En 1968 Wilson y Jungner llamaron la atención sobre el cribado al identificar 10 principios para guiar su uso.22 Con los conocimientos que hemos adquirido desde entonces, nos damos cuenta de que lo que habíamos pensado que era relativamente sencillo es mucho más complicado.
Notas
Puntos clave
▸ El diagnóstico precoz por sí mismo no está directamente relacionado con beneficio, a menos que pueda demostrarse una disminución de la enfermedad avanzada o de la mortalidad.
▸ El cribado tiene beneficios potenciales, pero no está exento de daños potenciales como el sobrediagnóstico. La comprensión de los posibles beneficios y daños debe preceder e informar la toma de decisiones compartida con los pacientes sobre el cribado.
▸ Dado que el cribado se centra en personas asintomáticas y que los resultados del cribado pueden conducir a la medicalización, es importante que los pacientes y los profesionales comprendan cuál es el beneficio (p. ej., mortalidad específica de la enfermedad) y su magnitud.
Lecturas recomendadas
Welch HG. Should I be tested for cancer? Maybe not and here’s why. Oakland, CA: University of California Press; 2006.
Welch HG, Schwartz LM, Woloshin S. Overdiagnosed. Making people sick in the pursuit of health. Boston, MA: Beacon Press; 2012.
Dickinson JA, Thériault G, Grad R, Bell NR, Szafran O. Assessing new screening tests. Panacea or profligate? Can Fam Physician 2022;68:815-22 (Eng), e310-7 (Fr).
Un pan como unas tortas
La Revista Cleveland Clinic Journal of Medicine ha publicado un comentario (versión traducida aquí ) donde aparte de poner de manifiesto la cuestiones dudosas o controvertidas del manejo clínico de la Vitamina D, avanza una sugestiva hipótesis que aclararía gran parte de esta interrogantes
Para los autores, el aumento más que exponencial en la petición de pruebas para determinar los niveles de vitamina D (25(OH)D) así como, la prescripción de suplementos de esta vitamina, se produce sin ningun fundamento real basado en la evidencia. Hay demasiados aspectos no aclarados en el manejo de esta «hipovitaminosis», desde la incertidumbre sobre el «punto de corte» del nivel adecuado de vitamina D, hasta la falta de respuesta de la suplementación con vitamina D en muchos de los procesos con los que presuntamente se asocia el déficit de esta vitamina.
En el articulo se explica que gran parte de esta confusión se debe a la presunción de que los niveles séricos de 25(OH)D reflejan el estado de la vitamina D.
¿Es posible que los niveles de vitamina D en sangre estén influidos por algo más que el estado de esta vitamina en el organismo?
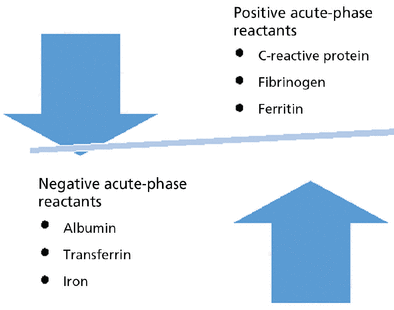
Si consideramos que la vitamina D es un reactante de fase aguda negativo, como se argumenta en el artículo, citando varios estudios y revisiones, los niveles bajos de 25(OH)D podrían reflejar simplemente perturbaciones metabólicas ligados a estados inflamatorios y no a un déficit real.
La elevada prevalencia de inflamación de bajo grado en la población general desaconsejaría por tanto, concluir de forma refleja que existe algún grado de insuficiencia o deficiencia de vitamina D cuando se encuentra una concentración sérica de 25(OH)D disminuida. Los estudios observacionales que encuentran asociaciones entre niveles bajos de vitamina D y el riesgo de fracturas, caídas, mortalidad, diabetes, hipertensión, COVID y una variedad de otros trastornos, podrían mostrar una mayor prevalencia de déficit de vitamina en estas enfermedades, aunque no se podría excluir la inversa, es decir que el déficit fuera consecuencia y no la causa de padecer estos trastornos. A la vista de estos argumentos, se concluye en contra de la prescripción rutinaria de suplementos de vitamina D, incluso cuando se encuentran niveles bajos de 25(OH)D.
Si los planteamientos de este articulo se probaran ciertos, la actitud actual de muchos de los médicos asistenciales de incluir la vitamina D en el petitorio de rutina de análisis clínicos, al igual que prescribir de forma indefinida vitamina D a sus pacientes cuando las cifras estuvieran por debajo de un limite (tan definido como incierto) seria hacer algo con gran desacierto o mal resultado.
En definitiva estaríamos haciendo un pan como unas tortas
Versión traducida del comentario en formato PDF aquí
Versión traducida de editorial del revista sobre el artículo en formato PDF aquí
Nirsevimab (Beyfortus®)
Por Juan Gérvas, Doctor en Medicina, médico general jubilado, ex-profesor de salud pública, Equipo CESCA, Madrid, España. jjgervas@gmail.com
Actualizado a 20 de septiembre de 2024, punto 6
Inyectar “nirsevimab” (Beyfortus ), un anticuerpo monoclonal, a recién nacidos y bebés para, preventivamente, evitar ingresos por bronquiolitis (por virus sincitial respiratorio)?
¡Pero si estos ingresos hospitalarios son pediatra-dependientes y Beyfortus no compensa beneficios con daños!
1. En mi pueblo
Cuando era médico rural, durante la semana los niños tenían catarro “que le había bajado” pero si no se había pasado la infección y seguían tosiendo, el viernes tenían bronquiolitis por virus sincitial respiratorio porque sabía que ese era el diagnóstico inevitable si la familia llevaba el bebé a urgencias al hospital.
De paso advertía: “Si lo lleváis a urgencias del hospital, para la bronquiolitis no hay tratamiento específico: no sirve adrenalina, ni antibióticos, ni corticoides, ni antitusivos, ni salbutamol, ni suelo salino hipertónico nebulizado, etc.”
Y “Lamentablemente, si vais a urgencias del hospital, el ingreso depende del pediatra que lo vea. Los hay que ponen la etiqueta a todos los niños para justificar su ingreso y los hay raros y sensatos que apenas ingresan con el diagnóstico de bronquiolitis”.
Y “Lo más importante, sigue dando el pecho que eso sí que evita bronquiolitis, neumonías, otitis y los ingresos y la mortalidad”.
Insistía en la lactancia al pecho porque se asocia a menos neumonías e infecciones en general de vías respiratorias bajas, menor mortalidad y también menos otitis media graves. El riesgo de hospitalización por infecciones de las vías respiratorias bajas como bronquiolitis en el primer año se reduce un 72% si los lactantes son amamantados exclusivamente durante más de 4 meses
Por cierto, justo el ingreso en el hospital de los bebés con la etiqueta de bronquiolitis conlleva en muchos casos la interrupción de la lactancia materna
2. En España, la bronquiolitis es una vergüenza
En España “bronquiolitis” es un diagnóstico que justifica ingresos con una variabilidad asombrosa, según zona geográfica.
Tenemos áreas sanitarias como Navalmoral de la Mata (en Cáceres) con 60 ingresos de bronquiolitis por 10.000 niños (en el año 2018). Al lado está Plasencia, con 443.
En Murcia, en la Vega Media del Segura los ingresos son 112 por 10.000 niños, y al lado Yecla-Jumilla tiene 800. En Lérida, en Pallars 917 ingresos, y al lado Alt Urgell 256.
[Por cierto, eche un ojo a este Atlas de Variaciones en Hospitalizaciones Pediátricas y localice su zona geográfica para hacerse idea de qué pie cojean sus pediatras].
No se ingresa por gravedad de la bronquiolitis, sino por los hábitos de los pediatras que trabajan dónde vive el bebé.
Como bien escribió un pediatra sensato, “La bronquiolitis es una vergüenza para la Pediatría”.
Se emplea todo medicamento que no se debe emplear ya que falla la ciencia, la ética y la profesionalidad. Además, se toman decisiones erróneas y dañinas con métodos diagnósticos como oximetría y radiografía de tórax, véase por ejemplo:
¿Hemos de poner suero salino hipertónico a los lactantes con bronquiolitis en Urgencias Pediátricas?
Manejo de la bronquiolitis aguda en atención primaria: análisis de variabilidad e idoneidad (proyecto aBREVIADo)
Effect of Oximetry on Hospitalization in BronchiolitisA Randomized Clinical Trial
Avoid doing chest x rays in infants with typical bronchiolitis
Por cierto, la mortalidad por bronquiolitis en España y los países desarrollados es prácticamente inexistente, aunque la propaganda del anticuerpo se base en que [el virus sincitial respiratorio] “es la segunda causa de muerte en el mundo en menores de un año”
3. “Nirsevimab” (Beyfortus)
Los anticuerpos monoclonales son medicamentos agresivos y caros («los medicamentos que llevan a los médicos a congresos más lejanos y lujosos»), que pueden tener graves efectos adversos. Entre ellos: reactivación de infecciones, enfermedad tiroidea, lupus eritematoso, dermatitis, cánceres, leucoencefalopatía, etc.
Beyfortus (nirsevimab) es un anticuerpo monoclonal humano de inmunoglobulina G1 kappa (IgG1κ) producido en células de ovario de hámster chino (CHO) mediante tecnología de ADN recombinante. De hecho, aunque en el ensayo clínico para prevenir los ingresos por bronquiolitis no hubo efectos adversos importantes, en la Ficha Técnica y en el prospecto de Beyfortus se advierte de que: «Este medicamento está sujeto a seguimiento adicional, lo que agilizará la detección de nueva información sobre su seguridad«
4. ¿Tenemos ya suficiente información para hacer la recomendación de introducir Beyfortus (nirsevimab)?
No
Unos pediatras sensatos revisaron la literatura y concluyeron
Así mismo, la evaluación con el método GRADE del ensayo clínico que “justifica” su venta (MELODY) concluyó que: “No se encontraron diferencias estadísticamente significativas entre ambos grupos [placebo y tratado], durante 150 días de seguimiento, en las variables:
1) Hospitalización, con prueba positiva a virus respiratorio sincitial, y
2) Hospitalización por todas las enfermedades respiratorias de cualquier causa»
Conviene tener en cuenta, también, la presión selectiva del medicamento sobre el virus. Es decir, la selección por el uso de nirsevimab de variedades del virus sincitial con mutaciones que le hagan resistente.
5. La tesitura de las familias españolas este otoño-invierno: “Si el pediatra sabe que no hemos inyectado al bebé con Beyfortus (nirsevimab), seguro que le diagnostica bronquiolitis y en urgencias lo ingresan por lo mismo”
Efectivamente, esa es la cuestión, que en muchos casos el ingreso por infección por virus sincitial respiratorio, bronquiolitis, es un “diagnóstico a posteriori” (se emplea para etiquetar justificar acciones sin ciencia ni ética). El diagnóstico va detrás de la decisión clínica, una irracionalidad frecuente por más que sea increíble. Como el ingreso por bronquiolitis es pediatra-dependiente, los bebés no inyectados con el anticuerpo monoclonal serán ingresados con más frecuencia que los inyectados. Es un sesgo de confirmación (todo lo que vemos parece confirmar lo que pensamos).
¡Pobres familias que tendrán que aceptar la inyección de Beyfortus (nirsevimab) a sabiendas de su negativo balance daños-beneficios!
6. HARMONIE
Actualización del 20 de septiembre de 2024
Se publicó el 27 de diciembre de 2023 un nuevo ensayo clínico, el HARMONIE, con bebés sanos, no enmascarado (los médicos y familiares sabían si el bebé había recibido la inyección del anticuerpo o de un placebo) y financiado por las industrias farmacéuticas (Sanofi y AstraZeneca), sin muertes. En un estudio previo, enmascarado, MELODY hubo cuatro bebés muertos entre los inyectados con el anticuerpo pero los investigadores consideraron que las muertes no tenían relación con el medicamento. Las cuatro muertes se produjeron en los días 140, 143, 286 y 338 tras la administración de nirsevimab. El análisis de los resultados de HARMONIE con el método GRADE revela un impacto ridículo pues se requiere inyectar de 171 a 1.334 bebés para evitar una hospitalización grave, y se logran 0,1 días añadidos de supervivencia libre de eventos.
Efectos adversos
A fecha de 15 de septiembre de 2024 se habían notificado 297 casos de sospechas de reacciones adversas a Beyfortus (nirsevimab) en EudraVigilance (el sistema europeo para declaración de sospechas de reacciones adversas), provenientes de Francia y España, la mayoría de ellas graves
Galicia
Se han publicado numerosos estudios observacionales (en la práctica clínica) sobre los resultados de las “campañas” de inmunización universal a los bebés con Beyfortus (nirsevimab) siendo particularmente importante el texto con los datos de Galicia, una de las primeras regiones del mundo en implantarla con carácter universal y gratuito. Los resultados son, aparentemente, muy favorables.
Sin embargo, el análisis GRADE de la efectividad del nirsevimab en bronquiolitis en Galicia demuestra que los bebés inmunizados ingresan con más gravedad lo que les lleva a más estancia en cuidados intensivos a los «inmunizados». De hecho, no hay diferencias entre inmunizados y no inmunizados respecto a “Hospitalización por Enfermedad Grave del TRI (tracto respiratorio inferior) relacionada con VRS (virus respiratorio sincitial)”, “sin/con ventilación mecánica invasiva Hospitalización por Enfermedad NO-Grave o Grave del TRI relacionada con VRS”. Hay un resultado dudoso favorable a favor de nirsevimab respecto a “Hospitalización por Enfermedad Grave del TRI relacionada con VRS, con aporte de oxígeno, y hay resultados en contra de nirsevimab respecto a “Hospitalización por Enfermedad Grave del TRI relacionada con VRS, que pasaron a cuidados intensivos”.
El estudio tuvo dos importantes sesgos: 1/ inmunizados, nirsevimab, más sanos 2/ de confirmación/expectativa
MedCheck
El Instituto de Farmacovigilancia de Japón ha revisado el uso de nirsevimab, por haberse introducido en su país. Su conclusión es la de no utilizar nirsevimab (Beyfortus®) para la prevención de la infección por virus sincitial respiratorio, para prevenir ingresos por bronquiolitis pues en el ensayo clínico MELODY disminuyó las hospitalizaciones pero incrementó las muertes. los estudios observacionales, todos muy favorables, tienen al menos tres importantes sesgos, de: 1/ niño sano, 2/ confirmación y 3/ clasificación
CONCLUSIÓN
Por todo lo expuesto, por favor, si a lo largo del año tras la inyección hay ingreso en UCI, muerte o cualquier otra sospecha de reacción adversa no deje de declararla (lo pueden hacer profesionales y legos)
No nos da tiempo
Traducción de BMJ 2023; 381:p1323 por Elisabeth Mahase doi: https://doi.org/10.1136/bmj.p1323

Esto suena importante: será mejor que retrase mi footing.
Puede que le apetezca sentarse, sobre todo si se encarga de transmitir a sus pacientes mensajes sobre estilos de vida saludables, como hacer más ejercicio, perder peso o dejar de fumar. La responsabilidad de mejorar la salud de la población parece recaer cada vez más en los médicos, sobre todo porque las políticas gubernamentales han fracasado en algunas cuestiones, como el control de la obesidad, a menudo por temor al «estatismo niñero «.
Ya estoy agotado
Eso es exactamente lo que sostiene un grupo de investigadores. Afirman que, aunque las intervenciones sobre el estilo de vida pueden ser eficaces, los médicos no tienen tiempo de aplicarlas, al menos en la situación actual de la sanidad.
¿Cómo salen las cuentas?
Los investigadores identificaron 57 directrices del NICE con 379 recomendaciones sobre intervenciones en el estilo de vida. Intentaron calcular el tiempo que se tardaría en llevar a cabo estas intervenciones -el tiempo necesario para tratar (TNT)- y los recursos humanos necesarios para aplicar las directrices. Clasificaron las intervenciones en «sencillas» (2,5 minutos), «intermedias» (15 minutos) o «complejas» (2,5 horas) y partieron del supuesto de que las intervenciones complejas serían realizadas por enfermeras, mientras que las sencillas y las intermedias corresponderían a los médicos de cabecera.
¿Necesito calentarme?
Ayudaría. En total, los investigadores calcularon que se necesitarían más de 45 000 horas de tiempo de médicos de cabecera y casi 300 000 horas de tiempo de enfermeras por cada 10 000 adultos para aplicar las 379 recomendaciones.
Es una maratón, no un sprint.
Y está muy por encima de la marca personal del NHS. Para aplicar los consejos se necesitarían siete veces más médicos de cabecera y 4,8 veces más enfermeras de las que hay actualmente. Incluso si todo el personal sanitario capacitado llevara a cabo las intervenciones, según los investigadores, el NHS necesitaría 2,6 veces más personal equivalente a tiempo completo.
¿Están exagerando las pruebas?
Quizá un poco. En su artículo publicado en BMJ Evidence-Based Medicine, los investigadores subrayan que sus cifras exactas deben «interpretarse con mucha cautela», ya que tuvieron que basarse en estimaciones. No obstante, sostienen que sus conclusiones deben ser tenidas en cuenta por los grupos de expertos a la hora de formular recomendaciones para el desbordado NHS.
Una guía en cuatro minutos de rudimentos sobre la salud y la asistencia sanitaria para los responsables de mantener los sistemas sanitarios.
Traducción de A four minute guide to the rudiments of health and healthcare for those responsible for maintaining health systems por Richard Smith, publicado en BMJ en https://doi.org/10.1136/bmj.p107
Salud y sanidad son cosas distintas
Las conversaciones sobre salud se convierten rápidamente en conversaciones sobre sanidad, pero la sanidad se ocupa sobre todo de la enfermedad. La salud no es un producto de los sistemas sanitarios.
La sanidad sólo representa el 10% de la salud
La salud es difícil, probablemente imposible, de definir, pero según cualquier definición la asistencia sanitaria sólo representa alrededor del 10% de la salud. La salud de las personas viene determinada por otros factores: sus circunstancias vitales, su entorno, sus genes y su estilo de vida, todos ellos entremezclados.
El aumento de la financiación sanitaria empeora paradójicamente la salud
Gastar más en sanidad desplaza la financiación de las prestaciones, las pensiones, la educación, la vivienda, el transporte público, el rediseño urbano, las artes, los deportes y otras actividades que son más importantes para la salud que la sanidad. Se crea así un círculo vicioso en el que una peor salud se traduce en más enfermedades que el sistema sanitario debe ayudar a tratar.
Los costes de la asistencia sanitaria aumentan sobre todo por las posibilidades de hacer más para responder a las enfermedades
Los costes de la sanidad han aumentado más deprisa que la inflación desde que se puso en marcha el SNS y otros sistemas sanitarios, principalmente a causa de las nuevas pruebas y tratamientos. Siempre se dice que los costes aumentan por el envejecimiento de la población, pero ese no es el principal factor, aunque son las personas mayores las que consumen la mayoría de las nuevas pruebas y tratamientos.
El aumento de la oferta es un importante motor de la demanda
Más médicos, más tratamientos, más pruebas y más camas de cuidados intensivos significan más actividad. Las unidades de cuidados intensivos se llenan igual que las nuevas carreteras y las nuevas cárceles, y la gente, sobre todo los moribundos, está ansiosa por someterse a tratamientos que pueden prolongar su vida (aunque a menudo no lo consiguen).
Una vida más larga va acompañada de periodos más largos de mala salud
En los años 80 nació una idea muy atractiva: la «compresión de la morbilidad». La idea era que la duración de la vida era fija -en torno a los 85 años- y que la mejora del entorno y de la asistencia sanitaria implicaría que las personas gozarían cada vez de mejor salud, comprimiendo el tiempo entre la aparición de la enfermedad y la inevitable muerte a los 85 años. La enfermedad se reduciría y los costes bajarían. Por desgracia, la «compresión de la morbilidad» sigue siendo una fantasía. La duración de la vida ha aumentado (hasta hace poco, cuando disminuyó para muchos) y el tiempo que se pasa con mala salud ha aumentado aún más.
La prevención no es más barata que el tratamiento, sobre todo a largo plazo
Principalmente por la razón descrita anteriormente, la prevención no suele ser más barata que el tratamiento, sobre todo a largo plazo.
Pocos pacientes se curan
Cuando se creó el SNS, la enfermedad se debía principalmente a enfermedades infecciosas y traumatismos, ambas potencialmente reversibles o «curables». Ahora, la mayor parte de la asistencia sanitaria se ocupa de personas con múltiples enfermedades de larga duración que no pueden curarse.
La división entre sanidad y asistencia social no tiene sentido
La mayoría de las muertes se deben ahora a la fragilidad (que podría llamarse vejez) y a la demencia. Estos pacientes al final de su vida necesitan cuidados, no tratamiento. Lo mismo ocurre con muchas personas discapacitadas. Tener asistencia sanitaria gratuita y cobrar por la asistencia social no tiene sentido, sobre todo con la capacidad de la asistencia sanitaria para consumir cada vez más recursos.
Hay grandes diferencias en todos los aspectos de la asistencia sanitaria
Dondequiera que se mire en la asistencia sanitaria -si la gente acude al médico por enfermedad, las derivaciones de los médicos de cabecera a los hospitales, las tasas de infección en los hospitales, las tasas de prescripción, los resultados de los tratamientos- se observa una enorme variación, la mayor parte de la cual no tiene explicación. Los intentos de reducir la variación han fracasado en gran medida.
El coste y la calidad de la asistencia sanitaria no están correlacionados
Si se paga más por un hotel o una botella de vino, se obtiene una experiencia mejor, pero no ocurre lo mismo con la asistencia sanitaria. La correlación entre coste y calidad es débil en la asistencia sanitaria, en parte por la enorme variación descrita anteriormente.
El bienestar de las personas con enfermedades de larga duración depende de ellas mismas y de sus cuidadores, no del sistema sanitario.
Si tiene meningitis, no será usted quien decida si vive o muere, sino los médicos. Pero por cada persona con meningitis hay decenas de miles con enfermedades de larga duración como diabetes, artritis, insuficiencia cardiaca y asma. Lo bien que les vaya a estas personas lo determinan principalmente ellas mismas y sus cuidadores: cómo reaccionan, qué comen, cómo hacen ejercicio y si cambian de vida y siguen sus tratamientos.
La mayoría de los cuidados no los prestan los profesionales sanitarios, sino la familia y los amigos.
Una persona que padece diabetes, cualquier enfermedad de larga duración o se está muriendo sólo ve a los profesionales sanitarios unas pocas horas al año. El resto del año deben ser atendidos por ellos mismos, sus familiares y amigos.
La asistencia sanitaria, en particular la hospitalaria, es peligrosa
Aproximadamente una de cada diez personas que ingresan en un hospital sufre un acontecimiento adverso, y aproximadamente una de cada cien morirá. La atención primaria es menos peligrosa.
La sanidad no puede reducir las desigualdades en salud
Las desigualdades en salud -por ejemplo, la diferencia de 15 años en la esperanza de vida entre ricos y pobres- vienen determinadas sobre todo por factores sociales (y políticos). La sanidad puede hacer poco contra las desigualdades.
Una mayor proporción de atención primaria respecto a la hospitalaria significa más satisfacción del paciente, mejores resultados y menores costes.
Los hospitales son la parte más cara del sistema sanitario y sistemáticamente se destina más dinero a los hospitales que a la atención primaria. Sin embargo, hace tiempo que sabemos que una mayor proporción de atención primaria respecto a la hospitalaria se traduce en una mayor satisfacción de los pacientes, mejores resultados y menores costes.
Traducción realizada con la versión gratuita del traductor http://www.DeepL.com/Translator
Tiempo necesario para tratar, algo que olvidan con frecuencia los hacedores de guías, protocolos y campañas de cribado
Resumen de Johansson M, Guyatt G, Montori V. Guidelines should consider clinicians’ time needed to treat BMJ 2023; 380 :e072953 doi:10.1136/bmj-2022-072953
El objetivo de las guías de práctica clínica es contribuir a una asistencia eficiente y de alta calidad. Se están haciendo esfuerzos para superar las barreras que dificultan su aplicación, como la falta de credibilidad por conflictos de intereses económicos o intelectuales, y la incapacidad de los clínicos para cambiar hábitos o mantenerse al día de las nuevas recomendaciones. Sin embargo, lo que rara vez se reconoce es que la aplicación de las directrices puede requerir un tiempo considerable por parte del clínico y, por lo tanto, tener considerables costes de oportunidad en el encuentro clínico. La inclusión de una evaluación del tiempo necesario para su aplicación podría modificar las recomendaciones de los comités de guías y ayudar a los médicos a establecer prioridades.
El objetivo de las guías de práctica clínica es contribuir a una asistencia eficiente y de alta calidad. Se están haciendo esfuerzos para superar las barreras que dificultan su aplicación, como la falta de credibilidad por conflictos de intereses económicos o intelectuales, y la incapacidad de los clínicos para cambiar hábitos o mantenerse al día de las nuevas recomendaciones. Sin embargo, lo que rara vez se reconoce es que la aplicación de las directrices puede requerir un tiempo considerable por parte del clínico y, por lo tanto, tener considerables costes de oportunidad en el encuentro clínico. La inclusión de una evaluación del tiempo necesario para su aplicación podría modificar las recomendaciones de los comités de guías y ayudar a los médicos a establecer prioridades.
Varios estudios han mostrado que es practicante imposible que en las jornada de un médico clínico se puedan aplicar todas la recomendaciones que las guías imponen. Es evidente que los médicos tienen que elegir qué recomendaciones seguir y en qué pacientes. Esto implica interpretar, priorizar y aplicar estas recomendaciones a un grupo diverso de pacientes con necesidades y deseos que pueden coincidir o no con las guías de práctica clínica. Pero sin orientación, y bajo la presión del tiempo, las decisiones sobre qué guías aplicar en el punto de atención serán implícitas, variables y potencialmente erróneas.
Una estrategia para resolver este problema consistiría en que los grupos de expertos estimaran el tiempo necesario para aplicar una intervención a la hora de determinar la orientación y la fuerza de las recomendaciones. Actualmente las guías más conocidas con contemplan este problema por lo que se proponemos que los organismos que crean las guías consideren explícitamente el «tiempo necesario para tratar» o «tiempo necesario para intervenir» (v del t).
El tiempo necesario para tratar (TNT) hace explícito el tiempo clínico estimado necesario para mejorar el resultado de una persona en la población diana (TNT -NNT), el tiempo clínico necesario para aplicar la recomendación a todas las personas elegibles en una consulta (TNT absoluto) y la proporción del tiempo clínico total disponible para la atención al paciente que se necesitaría para aplicar la recomendación a todos los pacientes elegibles (TNT relativo).
Los principales factores que afectan a las estimaciones del TNT. son:
- Tiempo necesario para proporcionar la recomendación a cada persona elegible
- Complejidad e intensidad temporal de la tarea
- Frecuencia con la que debe realizarse la tarea
- Herramientas y tecnología disponibles para facilitar la intervención
- Fracción de la población elegible
- Prevalencia de la enfermedad
- Umbral de elegibilidad
- Tiempo clínico disponible
- Número de médicos disponibles en el lugar donde se va realizar la recomendación
- Quién aplicará la recomendación
- Proporción de horas clínicas disponibles para la atención al paciente en la consulta
Los autores calculan el TNT absoluto en el caso de poner en marcha la guía NICE sobre «Actividad física: consejos breves para adultos en atención primaria». Si se siguieran las directrices de esta guía el TNT absoluto en una consulta de 2000 adultos seria, de 10 000 minutos, o 167 horas, de tiempo de un General Practitioner. Trasladado a España un médico de familia necesitaría casi 24 días (más de un mes) a tiempo completo par al año para poner en marcha estas recomendaciones.
Inclusión del tiempo en las directrices
Junto con otros factores relevantes, los grupos de elaboración de directrices deben tener en cuenta las estimaciones de el TNT a la hora de decidir si recomiendan una intervención y con qué intensidad. Para ayudar a los grupos de expertos a hacerlo, los marcos de elaboración de guías (como GRADE ) deberían establecer cómo tener en cuenta el tiempo que los médicos dedican a la aplicación de estas.
Considerar explícitamente el tiempo del clínico estimando el TNT podría convertir una «recomendación fuerte a favor» en una débil o incluso convertir una «recomendación débil a favor» en una «recomendación débil en contra». Las TNT pueden resultar especialmente útiles cuando las directrices hacen recomendaciones que se aplican a una gran fracción de la población general y cuando los efectos beneficiosos de la intervención recomendada son pequeños, en términos absolutos.
Los autores de las guías deberían considerar de forma rutinaria el tiempo necesario para llevar a cabo intervenciones de rendimiento relativamente bajo aplicadas a grandes proporciones de la población. De este modo, el entusiasmo por este tipo de intervenciones disminuirá, y las recomendaciones fuertes pasarán a ser débiles, y las recomendaciones a favor pasarán a ser contrarias. El resultado neto aliviará a los médicos de conjuntos imposibles de recomendaciones y aumentará el beneficio neto de la atención que prestan
Disminuir la accesibilidad inmediata y trasladar trabajo
Por Rafael Bravo Toledo. Publicado como parte de la sección Un vistazo a las últimas publicaciones de AMF 2022;18(7):428-430
Muchos pacientes, no reciben los cuidados agudos, crónicos y preventivos recomendados por las guías. Una explicación obvia, aunque olvidada, es que los profesionales de atención primaria dispongan del tiempo suficiente para brindar esa atención.
Aunque es un lugar común, esta es la frase de comienzo de un artículo donde se repasa el tiempo necesario para proporcionar los cuidados de atención primaria, que, según los estándares de atención, necesita la población adulta.
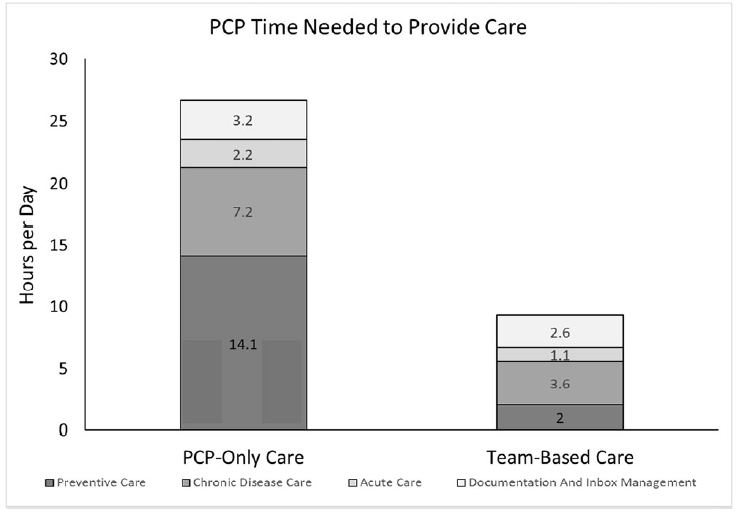
Partiendo de un hipotético cupo de 2500 pacientes representativos de la población, se estimó que un médico necesitaba 26,7 h/día para realizar estas actividades, este tiempo se distribuía en: 14,1 h/día para la atención preventiva, 7,2 h/día para la atención de enfermedades crónicas, 2,2 h/día para la atención aguda y 3,2 h/día para trámites burocráticos y gestión de la demanda.
Cuando la atención pasaba a ser realizada en equipos de atención primaria específicos basados en equipos (team-based care en el original), se estimó que se requerían 9,3 h por día (2,0 h/día para la atención preventiva y 3,6 h/día para la atención de enfermedades crónicas, 1,1 h/día para la atención aguda y 2,6 h/día para la burocracia).
Ver Figura: Tiempo que un proveedor de atención primaria necesita para atender a un cupo medio de 2.500 pacientes adultos en EE.UU. Tomada de Porter, J., Boyd, C., Skandari, M.R. et al. Revisiting the Time Needed to Provide Adult Primary Care. J Gen Intern Med 2023; 38;:147–155. https://doi.org/10.1007/s11606-022-07707-x
La conclusión, obvia: los profesionales no tienen tiempo suficiente para proporcionar la atención primaria recomendada por las guías y/o estándares. Con la atención basada en equipos, las necesidades de tiempo disminuirían en más de la mitad, pero seguirían siendo excesivas.
¡Bien! hemos encontrado justificación, escrita y en inglés, para perpetuar nuestro lamento sobre la falta de tiempo.
¡Para! Que igual no es así, veamos.
En el modelo, el “mejor escenario” comprende un cupo de 1500 pacientes, atención por equipo, 5 min por visita de enfermedad crónica, una proporción de tiempo entre atención crónica y aguda del 75%, y un 30% del tiempo para burocracia realizada por otros miembros del equipo.
Casualmente es similar con las condiciones de un médico de familia que trabajara en un hipotético centro de salud español.
En este “mejor caso” el médico necesitaría 4.5 h/ día.
También curioso que se acerque al tiempo estándar de un médico en un centro español, aunque nuestra experiencia “sentida” nos diga que esto no es así. Si repasamos de nuevo el articulo podemos averiguar las características diferenciales entre el modelo propuesto y el nuestro, sin olvidar que otras diferencias entre sistemas sanitarios podrían explicarlo.
La primera es la desigualdad en la atención a proceso agudos ya que en el modelo calculó, a partir de estudios representativos, unas 637 visitas por cada 1000 pacientes adultos por año. En nuestro país y tomando los datos de un estudio reciente, la frecuentación se estima en 4,2 vistas por paciente y año; este dato multiplicaría por siete el tiempo de atención, una diferencia excesiva incluso considerando un tiempo de atención de estos procesos en el modelo propuesto superior a 20 minutos. Otra causa importante era la idea de que otros miembros del equipo podrían asumir una parte importante del tiempo dedicado a actividades preventivas, manejo de la enfermedades crónicas y agudas, así como del tiempo dedicado a burocracia y manejo de la demanda.
En el articulo se plantean varios modelos basándose en que el cupo tenga mas o meno pacientes y alterando los tiempos de dedicación de los médicos y de los otros miembro del equipo. En todos los casos, la conclusión fue la misma: la prestación de los servicios ideales de prevención, enfermedades crónicas y cuidados intensivos basados en directrices supone una carga de tiempo excesiva para el médico de familia que sólo se ve parcialmente mitigada por los modelos de atención basados en equipos y los paneles de menor tamaño.
En definitiva, una conclusión provocativa que traiciona la frase inicial, se podría decir que disminuir la accesibilidad (inmediata) y fomentar activamente la participación de otros profesionales haría posible prestar sin tantos problemas de tiempo, las actividades preventivas, atención a enfermos crónicas y agudas de un cupo de hasta 2500 personas por parte de los médicos de familia.