Etiquetado: antivirales
Paxlovid, ¿Otro Tamiflu?
EPIC-HR: Algunos datos decepcionantes sobre Paxlovid
Traducido del original de Morgenstern, J. EPIC-HR: Some underwhelming data on Paxlovid. First10EM, April 12, 2022. Disponible en : https://doi.org/10.51684/FIRS.127210
Mi inicial actualización sobre la evidencia para Paxlovid (nirmatrelvir/ritonavir) no contenía exactamente ninguna evidencia, porque no se había publicado nada, a pesar de las recomendaciones en ese momento de múltiples organizaciones. Lamentablemente, dos años después de la pandemia, una gran parte de la comunidad médica todavía parece dispuesta a actuar basándose únicamente en los comunicados de prensa de las compañías farmacéuticas. El ensayo EPIC-HR ya ha sido publicado, por lo que al menos podemos discutir la ciencia, que desafortunadamente es un pequeño desastre. Al final del día, no estoy más seguro de que Paxlovid realmente ayude de lo que estaba antes de que se publicara este ensayo.
El artículo
Hammond J, Leister-Tebbe H, Gardner A, Abreu P, Bao W, Wisemandle W, Baniecki M, Hendrick VM, Damle B, Simón-Campos A, Pypstra R, Rusnak JM; EPIC-HR Investigators. Oral Nirmatrelvir for High-Risk, Nonhospitalized Adults with Covid-19. N Engl J Med. 2022 Feb 16:NEJMoa2118542. doi: 10.1056/NEJMoa2118542.
Métodos
Se trata de un ECA doble ciego controlado con placebo de fase 2/3.
Pacientes
Pacientes adultos con COVID-19 confirmado y sintomático, dentro de los 5 días posteriores al inicio de los síntomas, y al menos una característica de alto riesgo de progresión a enfermedad grave.
Exclusiones: vacunación COVID, infección previa por COVID, necesidad anticipada de hospitalización dentro de los 2 días, recepción de plasma convaleciente.
Intervención
Paxlovid (nirmatrelvir más ritonavir 300mg/100mg) por vía oral cada 12 horas durante 5 días.
Comparación
Placebo.
Outcome
El resultado primario fue una variable compuesta de mortalidad por todas las causas y hospitalización específica por la enfermedad a los 28 días. Utilizaron un análisis modificado de intención de tratar que solo incluyó a pacientes que recibieron el medicamento dentro de los 3 días posteriores al inicio de los síntomas, a pesar de sus criterios de inclusión.
Resultados
Se recluto a 2246 (de 3000 pacientes previstos). La mediana de edad fue de 46 años, el 51% eran hombres, el 80% tenían un IMC superior a 25, el 39% eran fumadores y el 33% tenían hipertensión. El 66% dentro de los 3 días posteriores al inicio de los síntomas.
Para su resultado primario compuesto de hospitalización por COVID-19 o muerte, hubo una reducción significativa con el tratamiento (0,7% vs 6,5%). Los resultados son similares en su análisis secundario que analiza a todos los pacientes (hasta 5 días después del inicio de los síntomas): 0.8% vs 6.3%.
No presentan datos sobre las cifras generales de mortalidad. Hubo 0 muertes en el grupo de tratamiento y 9 (1,3%) en el grupo de placebo.
No presentan números globales absolutos de hospitalización
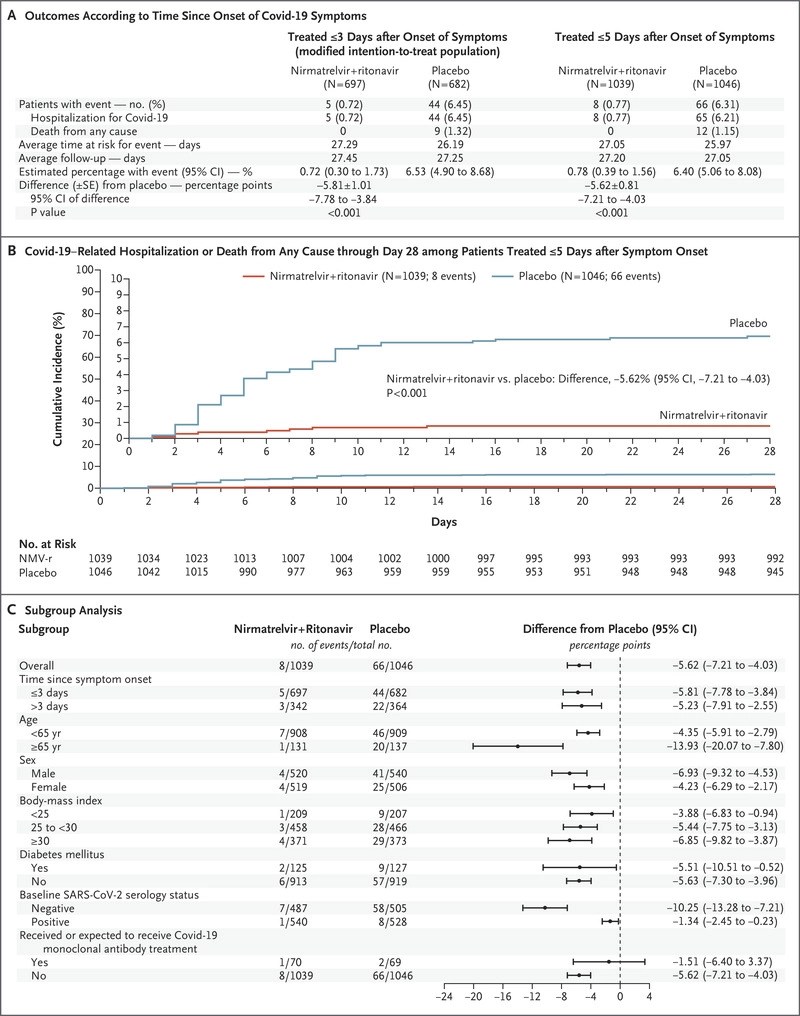
No hay una diferencia en los eventos adversos informados, pero cuando los eventos adversos están ocurriendo en el 25% de ambos grupos, y puede ser difícil detectar una señal de daño de un agente experimental novedoso más pequeña.
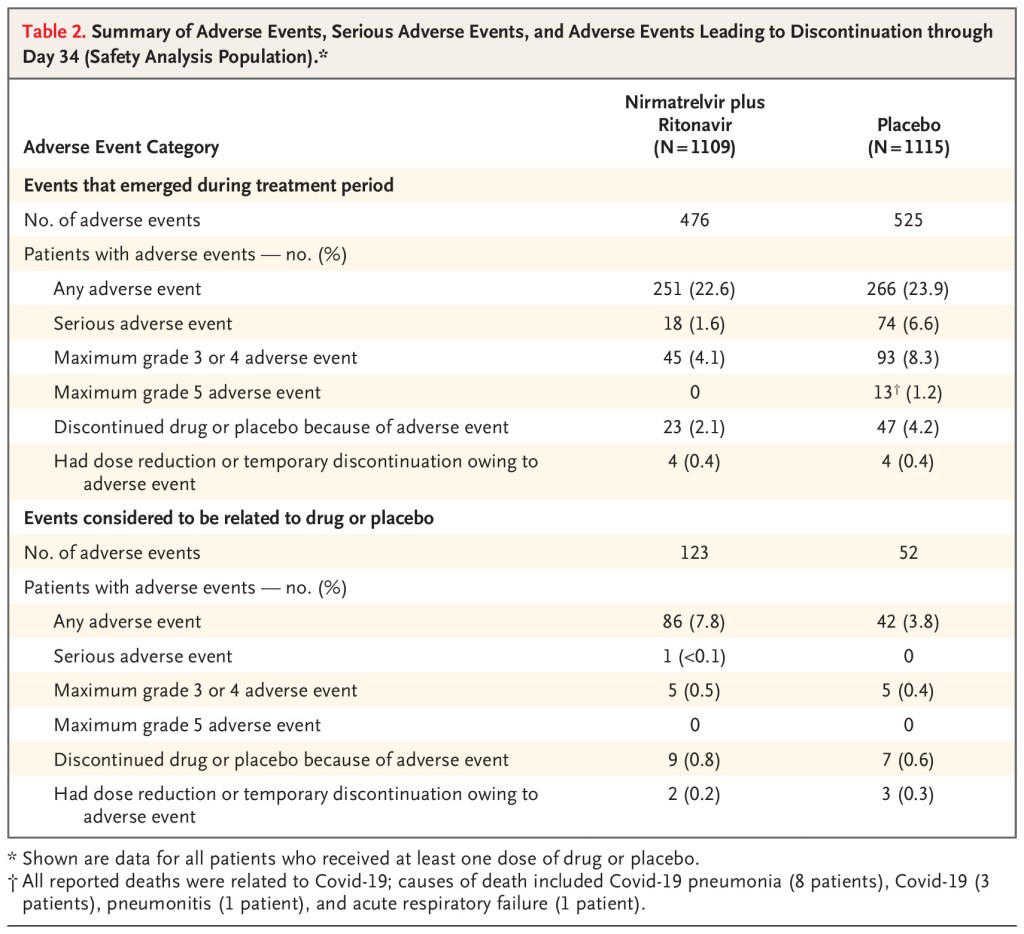
Mis pensamientos
A pesar de que este es un ECA doble ciego con resultados prometedores que entusiasman a muchas personas, este ensayo tiene muchos problemas que me dejan muy inseguro sobre los resultados.
Este ensayo está completamente dirigido por Pfizer. El primer autor, el autor senior y muchos de los otros autores son empleados de Pfizer. Por lo tanto, hay un conflicto de intereses masivo que debe ser considerado. Como discuto en mi bibliografía de EBM, los estudios patrocinados por la industria (por no hablar de si son diseñados y ejecutados) tienen muchas más probabilidades de encontrar resultados positivos para sus propios productos. Existe evidencia empírica de que estos estudios de la industria son sesgados o tramposos. (Por ejemplo, Lexchin 2003) Por lo tanto, siempre debemos rebajar nuestra confianza en los estudios con conflictos de intereses tan obvios. Si, sin el conflicto de intereses, leyó este estudio y pensó que había un 60% de posibilidades de que Paxlovid funcione, el conflicto de intereses significa que probablemente necesite reducir esa estimación a menos del 40%, y tal vez mucho más. (Por supuesto, esos números están completamente inventados). La replicación siempre es esencial en medicina, pero mucho más cuando la persona que dirige el ensayo también está tratando de venderle algo.
Ha sido un problema recurrente en la investigación de COVID, pero este ensayo utiliza el resultado increíblemente sesgado y completamente irrelevante de las «hospitalizaciones relacionadas con COVID-19». Esto transforma un resultado relativamente objetivo en uno completamente subjetivo. Significa que los pacientes pueden ser admitidos en el hospital por reacciones graves a los medicamentos, y simplemente ser ignorados. Y significa que el manuscrito nos proporciona un número sin sentido. No nos dice cuántas personas fueron admitidas en el hospital, que es el resultado que realmente les importa a los médicos y pacientes. Solo nos dice el subconjunto de admisiones que pensaron que se debían a COVID (que todos sabemos que es increíblemente difícil de distinguir). Encuentro esto especialmente problemático en este ensayo, porque ni siquiera presentan los números de hospitalización por todas las causas. (ni siquiera enumeran los números reales de hospitalización en el suplemento). No hay forma de saber a partir de este manuscrito si paxlovid disminuyó las hospitalizaciones totales, que es el único supuesto beneficio. (Para el caso, basado en esta publicación, es muy posible que Paxlovid realmente aumente las hospitalizaciones. Con base en el número de «hospitalizaciones relacionadas con COVID» y el número de eventos adversos enumerados, dudo que esto sea un problema, pero simplemente no hay forma de saberlo).
En comparación con el resultado completamente irrelevante, subjetivo y sesgado de la hospitalización específica de la enfermedad, la reducción del 1,3% en la mortalidad definitivamente sería clínicamente importante. No entiendo por qué no presentan estadísticas para este hallazgo. (Cuando conecto los números a una calculadora en línea, obtengo un valor de p de 0.002 para este resultado). En mi opinión, este número es realmente la única parte prometedora del manuscrito publicado. Las otras fuentes de sesgo aún limitan mi certeza, y solo se aplica a un grupo muy selecto de pacientes que en su mayoría no se parecen a los pacientes que estoy viendo, pero el beneficio potencial de mortalidad es un hallazgo que vale la pena perseguir en futuras investigaciones.
Utilizaron un análisis modificado de intención de tratar que solo incluyó a pacientes que recibieron el medicamento dentro de los 3 días posteriores al inicio de los síntomas, a pesar de incluir pacientes hasta 5 días después del inicio de los síntomas. Su plan estadístico no se describe en ninguna parte del registro del ensayo, y realmente no explican por qué limitaron su análisis estadístico a los pacientes dentro de los 3 días posteriores a los síntomas a pesar de incluir a los pacientes a 5 días. Nunca he visto un estudio ajustar sus criterios de inclusión dentro de su análisis estadístico de esa manera, y en un estudio dirigido por la industria, me preocupa el potencial p-hacking..
El ensayo se detuvo temprano, inscribiendo a 2246 de los 3000 pacientes planificados. (el número se hace aún más pequeño, porque solo incluyeron a 1379 pacientes en su intención modificada de tratar el análisis). Se detuvieron en un análisis intermedio planificado, pero la terminación anticipada significa que es probable que el beneficio se sobreestime.
Hay una serie de resultados secundarios enumerados en el registro del ensayo, como la duración de los síntomas, la gravedad de los síntomas, la duración de la estancia hospitalaria y la duración de la estancia en la UCI, que no se enumeran en el manuscrito, que es una forma de sesgo de publicación. (Teniendo en cuenta que Pfizer es quien escribe estos resultados, puede apostar que estos resultados se habrían enumerado si hubieran hecho que Paxlovid se viera bien).
Como discuto en el largo interludio filosófico del artículo de budesonida, debemos tener en cuenta la probabilidad previa a la prueba al evaluar nuevos estudios. Durante la pandemia, hemos arrojado tantos productos químicos diferentes como COVID-19, que debemos esperar que una serie de estudios sean positivos solo por casualidad. (El siguiente gráfico de una publicación reciente en Nature da una buena idea de la baja probabilidad previa a la prueba requerida para cualquier agente individual). Por lo tanto, un solo estudio positivo nunca será completamente convincente. Cuando se agrega el hecho de que este es un estudio dirigido por la industria con un resultado primario que es inherentemente problemático, creo que hay menos de un 50% de posibilidades de que estos hallazgos se repliquen en investigaciones independientes de alta calidad.
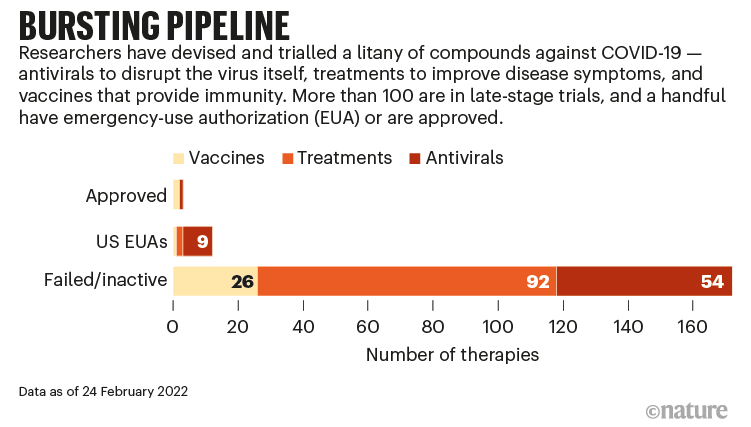
Imagine modified from: https://www.nature.com/articles/d41586-022-00562-0
En última instancia, simplemente no estoy seguro de qué hacer con estos datos. Fuera de una pandemia, creo que está muy claro que no recomendaríamos este medicamento en este momento, y en su lugar exigiríamos más evidencia. Un ensayo de la industria con tantos problemas simplemente no es suficiente para sostener la práctica de manera segura. Sin embargo, la pandemia puede cambiar las matemáticas, y el hallazgo de mortalidad podría ser importante. (Honestamente, no sé si la pandemia debería cambiar nuestras decisiones. Me preocupa abandonar nuestros principios básicos de MBE. Si estamos usando diferentes cálculos durante la pandemia, creo que es esencial que lo dejemos completamente claro, porque de lo contrario estas prácticas se afianzarán para siempre, incluso cuando la pandemia finalmente haya terminado).
Teniendo en cuenta la alta probabilidad de que futuras investigaciones independientes refuten estos hallazgos, debemos tener mucho cuidado al decidir quién debe recibir este medicamento. Si quisieras argumentar que no deberíamos prescribirlo en absoluto, probablemente no se necesitaría mucho para convencerme de que tienes razón. Sin embargo, suponiendo que lo vamos a prescribir en base a estos resultados inciertos pero prometedores, la incertidumbre significativa significa que realmente deberíamos limitar las prescripciones a la población en la que se estudió. Los datos no parecen lo suficientemente fuertes como para extrapolarlos a otras poblaciones no estudiadas. Por lo tanto, hasta que se publiquen más estudios, creo que los únicos pacientes que deben considerarse para paxlovid son adultos no vacunados con COVID-19 confirmado, dentro de los 5 días posteriores al inicio de los síntomas y con al menos un criterio de alto riesgo para la progresión a COVID-19 grave.
Hay un segundo ECA que se ha informado a través de un comunicado de prensa. Basado en el registro del ensayo, el ensayo EPIC-SR analizó a pacientes de riesgo estándar y se centró en la resolución de los síntomas en lugar de los resultados duros. (Suena como Tamiflu.) Probablemente lo cubriré cuando se publique, pero basándome en el hecho de que es esencialmente un espejo de este estudio, dirigido por Pfizer, espero que muchos de los problemas sean los mismos.
(Creo que haríamos bien en recordar cuánto dinero se gastó durante el H1N1 en el «medicamento milagroso» Tamiflu, y qué tan bien resultó).
En conclusión
Teniendo en cuenta el conflicto de intereses financieros y las múltiples fuentes significativas de sesgo, creo que se trata de evidencia de baja calidad. El único beneficio reclamado es un resultado sesgado, subjetivo y completamente no orientado al paciente. Fuera de una pandemia, definitivamente no recetaría Paxlovid. Si cree que esta evidencia es lo suficientemente fuerte como para justificar el tratamiento dependerá mucho de cuánto piense que una pandemia cambia las reglas de la medicina basada en la evidencia.
Referencias
Hammond J, Leister-Tebbe H, Gardner A, Abreu P, Bao W, Wisemandle W, Baniecki M, Hendrick VM, Damle B, Simón-Campos A, Pypstra R, Rusnak JM; EPIC-HR Investigators. Oral Nirmatrelvir for High-Risk, Nonhospitalized Adults with Covid-19. N Engl J Med. 2022 Feb 16:NEJMoa2118542. doi: 10.1056/NEJMoa2118542. Epub ahead of print. PMID: 35172054
Lexchin J, Bero LA, Djulbegovic B, Clark O. Pharmaceutical industry sponsorship and research outcome and quality: systematic review. BMJ. 2003 May 31;326(7400):1167-70. doi: 10.1136/bmj.326.7400.1167. PMID: 12775614
Interactuando
Juan, médico de familia que trabaja en un centro de salud de un servicio de salud autonómico nos envía el siguiente caso que ilustra un problema de seguridad cuya causa principal sería el (mal) diseño y funcionalidad de la historia clínica electrónica.
Acude a consulta sin cita y por motivo urgente, José Carlos cojeando y con dolor en tobillo derecho tras caerse mientras practicaba running la noche anterior. A la exploración aparece un tobillo hinchado con dolor la palpación en maléolo externo camina más de cuatro pasos, aunque le cuesta apoyar el pie afectado y poner peso sobre él. Ante la positividad de uno más ítems de la reglas de Ottawa se le pide radiografía urgente en la que no se observan líneas de fractura.
Con el diagnostico de Esguince tobillo grado II se le recomienda a José Carlos, el siguiente tratamiento: reposo evitando apoyar peso en el tobillo lesionado, aplicación local de hielo durante los primeros días cada 3 o 4 horas durante 20 a 30 minutos seguidos, inmovilización del tobillo con vendaje funcional y elevación del miembro afecto cuando este sentado o tumbado. Así mismo se le recomienda Naproxeno 550 un comprimido cada 12 horas durante cinco días para aliviar el dolor y reducir la hinchazón del tobillo.
 Cuando José Carlos se dispone a abandonar la consulta, Juan repasa en la pantalla y advierte que José Carlos esta diagnosticado de VIH +, como el seguimiento y tratamiento de dicha afección es hospitalario no consta ningún dato en la historia clínica del centro de salud, aunque por fortuna su médico incluyó en su momento el epígrafe diagnóstico.
Cuando José Carlos se dispone a abandonar la consulta, Juan repasa en la pantalla y advierte que José Carlos esta diagnosticado de VIH +, como el seguimiento y tratamiento de dicha afección es hospitalario no consta ningún dato en la historia clínica del centro de salud, aunque por fortuna su médico incluyó en su momento el epígrafe diagnóstico.
¿Estas tomando algo para tu problema del VIH? ¿le pregunto Juan, a José Carlos?
Si, Atripla*
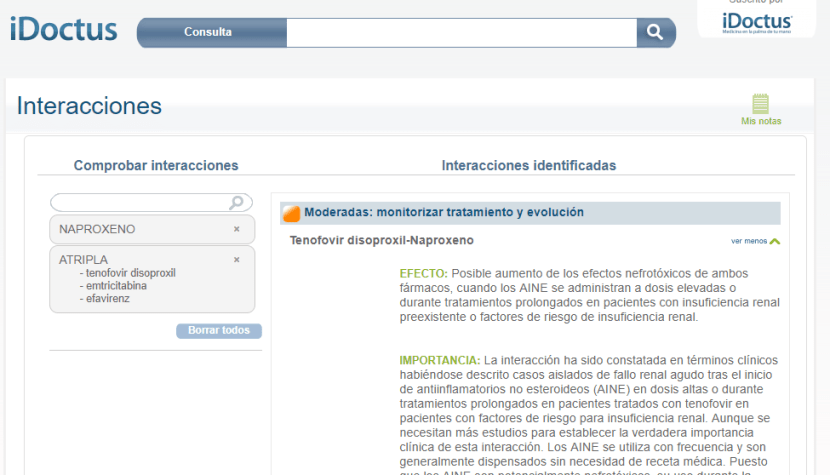
Juan, echa un vistazo a una página web externa de interacciones (el programa de su historia clínica electrónica no las incluye a pesar de reiteradas peticiones) y observa esto
La interacción es “moderada” pero Juan decide suprimir el antinflamatorio y prescribir un analgésico en caso de dolor.
*[Atripla] es una mezcla de medicamentos efavirenz, emtricitabina y tenofovir y que se toma en un solo comprimido. Como Altipra es de “Diagnóstico hospitalario” ** no aparece entre los tratamientos farmacológicos de José Carlos.
** Se considera de Diagnóstico hospitalario aquellas especialidades farmacéuticas en las que, por las características de los principios activos que entran en su composición, por sus indicaciones específicas, por las condiciones especiales requeridas para su aplicación o por necesitarse un control continuado de efectos y resultados, la prescripción, dispensación y administración controlada debe hacerse bajo la responsabilidad del hospital.
siete dias

Habría que modificar la conocida frase La gripe sin tratamiento dura una semana, con tratamiento siete días; por esa otra La gripe sin tratamiento dura siete días, con Tamiflu seis días y medio
Resumido de Reuters :Según un estudio, publicado en la revista Lancet Infectious Diseases, que revisó muchos estudios diferentes publicados sobre Tamiflu y Relenza, se vio que ambos medicamentos ahorran alrededor de medio día, en promedio, del tiempo que los pacientes sufren la enfermedad. La influenza usualmente afecta a las personas por alrededor de una semana.
Por otro lado segun se puede leer en el British Medical Journal menos de la mitad de los 8.500 profesionales sanitarios entrevistados sobre su disposición a ponerse la vacuna contra el virus A se mostró partidario de recibirla.