Etiquetado: Publicacióncientifica
y una revisión sistemática
Las revisiones sistemáticas RS y en concreto las de la Cochrane sirven para algo más que con  voz campanuda decir “una revisión de la Cochrane dice que …..” . Sirven sobre todo para sintetizar de forma organizada y científica las respuestas a las preguntas que se hacen en la clínica. Aparte de coronar la jerarquía de la evidencia científica, otras cualidades de las RS son la de facilítanos el acceso y recopilación de la gran cantidad de información científica que se publica, la de actualizar, reunir y compendiar toda la información sobre un tema concreto, la de crear nuevas evidencias ante resultados previos inconsistentes y algunas más.
voz campanuda decir “una revisión de la Cochrane dice que …..” . Sirven sobre todo para sintetizar de forma organizada y científica las respuestas a las preguntas que se hacen en la clínica. Aparte de coronar la jerarquía de la evidencia científica, otras cualidades de las RS son la de facilítanos el acceso y recopilación de la gran cantidad de información científica que se publica, la de actualizar, reunir y compendiar toda la información sobre un tema concreto, la de crear nuevas evidencias ante resultados previos inconsistentes y algunas más.
Además y como bien dice el titulo de una carta publicada en Lancetdeben ser el principio y el final de un buen ensayo clínico: Clinical trials should begin and end with systematic reviews of relevant evidence,
Lo explicamos: cualquier asistente a un cuso de metodología de la investigación o de cómo redactar un articulo biomédico, lo primero que aprende es que la justificación y el objetivo del estudio se plasma en la primera parte o introducción que debe ir encabezada con un resumen breve , casi telegráfico, de lo que se sabe sobre el tema: el estado del arte en sentido aristotélico….
¡qué mejor forma que sustentarlo y referenciarlo que con una revisión sistemática.
“Para justificar un nuevo ensayo clínico tanto científica como éticamente debe concebirse a la luz de una evaluación de investigaciones anteriores, lo ideal sería una revisión sistemática”
Así mismo, nos han enseñado y así lo creemos (con permiso de Manuel Arranz que pone en tela de juicio la estructura de un original científico y lo hace de forma comprometida y humoristica en una antigua serie de la revista Gestión Clínica y Sanitaria) que en la parte final, la discusión se debe confrontar nuestros resultados con los de trabajos previos. De nuevo que mejor que una revisión sistemática para tener localizados, referenciados y adecuadamente tabulados estos estudios y estos resultados.
“Cuando se dan a conocer los resultados, estos deben establecerse en el contexto de la revisión actualizadas de otras investigaciones similares.”
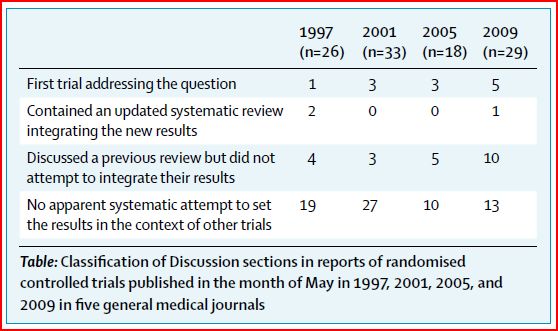
Los autores de la carta del Lancet evaluaron en tres artículos publicados en 1997, 2001 y 2005 los ensayos aleatorios publicados en el mes de mayo en cinco revistas médicas: Annals of Internal Medicine, BMJ, JAMA, The Lancet y el New England Journal of Medicine. Sólo una pequeña proporción de los informes de estos ensayos proporcionaban información suficiente para evaluar la contribución de los nuevos resultados a la totalidad de la evidencia disponible. Repite ahora el estudio (mayo de 2009) y como en las publicaciones previas evaluaron las secciones de discusión de los ensayos y vieron en qué medida los ensayos referencian revisiones sistemáticas en la sección de introducción. Los resultados son estos:
A la vista de estos desesperanzadores datos los editores del Lancet y de acuerdo con las recomendaciones CONSORT (Consolidated Standards of Reporting Trials), han decidido pedir a los autores que pongan su trabajo en “el contexto de lo que ha pasado antes”.
Por tanto los artículos remitidos para publicación a The Lancet a a partir de agosto deben incluir una revisión sistemática de la investigación previa en la sección de discusión e incluir en esta misma sección una confrontación de su resultados con las de los estudios localizados mediante la revisión como se puede ver en la tabla  y como aparece – lo ponen como ejemplo- en el estudio TACT Sequential docetaxel as adjuvant chemotherapy for early breast cancer (TACT): an open-label, phase III, randomised controlled trial.
y como aparece – lo ponen como ejemplo- en el estudio TACT Sequential docetaxel as adjuvant chemotherapy for early breast cancer (TACT): an open-label, phase III, randomised controlled trial.
Gracias a Sergio Uribe por ponerme en las pista de esta información.