Categoría: Pendiente
la pandemia
Pandemia de gripe A: incoherencias y falta de transparencia
por Juan Gérvas.
- La gripe A empezó en Méjico, en abril de 2009, de origen porcino. En junio de 2009 la Organización Mundial de la Salud (OMS) declaró la situación de máxima alerta, “pandemia” nivel 6. Tal término (“pandemia”) desencadenó la activación de contratos “dormidos” de los Gobiernos con la industria farmacéutica y permitió establecer planes con controles mínimos para la producción de vacunas antigripales contra el nuevo virus. “Pandemia” significaba ya sólo afectación mundial, sin asociación a gravedad ni mortalidad.
- Las predicciones de la OMS fueron desde el principio y hasta el final de gran catástrofe. De hecho, se activaron “planes de contingencia” similares a los de la gripe Aviar de 2005 (en que se previeron también erróneamente millones de muertos). Sólo el Gobierno de Polonia resistió las presiones, y no firmó contratos que implicaban aceptar todas las responsabilidades por los daños que causaran las nuevas vacunas. Su respuesta racional conllevó el mismo número de muertos por gripe A que en el resto de Europa (181 en Polonia, con 39 millones de habitantes, frente a, por ejemplo, España con 47 millones de habitantes y 271 muertos). También fallaron las predicciones de pacientes ingresados en Cuidados Intensivos, que fueron de miles frente a cientos en la realidad. Frente a estos datos, la OMS y las autoridades sanitarias siguen hablando de “nuevas olas” amenazadoras, anunciando un Fin del Mundo que sustente su respuesta según “el principio de precaución”.
- La gripe A causó una epidemia de gripe leve, y la mayoría de los enfermos no tuvieron ningún síntoma. Tal levedad se conocía con certeza y datos fiables desde mayo de 2009. Se calcula que más de la mitad de la población tiene ahora, en 2010, defensas naturales frente a la gripe A (antes de la 2009 sólo tenían defensas aproximadamente un 30% de los nacidos antes de 1957, pues el virus A fue predominante entre 1919 y 1957).
- Se recomendaron tratamientos antivirales de dudosa eficacia.
- Se recomendaron vacunas de dudosa eficacia. De hecho la vacuna contra la gripe estacional (triple vírica, con virus atenuados) sensibilizó para tener con más probabilidad la gripe A. Además, el virus de la gripe A desplazó a todos los previos por lo que la vacuna contra la gripe estacional fue inútil.
- La población y los profesionales sanitarios europeos (y españoles) rechazaron las medidas propuestas por las autoridades sanitarias, y no se vacunaron en masa. La incoherencia de las autoridades españolas se demuestra, por ejemplo, con la distinta definición de caso de gripe A en las distintas Comunidades Autónomas (hubo, pues, “gripe A catalana”, “gripe A vasca”, etc.).
- La Unión Europea y el Consejo de Europa han expresado su malestar por la hiper-reacción y la falta de transparencia de las autoridades sanitarias. En EEUU preocupa que la Directora de los CDC (organizaciones oficiales para el control y seguimiento de epidemias y vacunas) haya pasado a Presidente de la Sección de Vacunas de Merck (industria farmacéutica que fabrica vacunas).
- Conviene que la población y los profesionales sanitarios tengan criterio propio, pues el de las autoridades puede ser errado, y además no enmendado
la pandemia de gripe desde el punto de vista clínico
ya es primavera
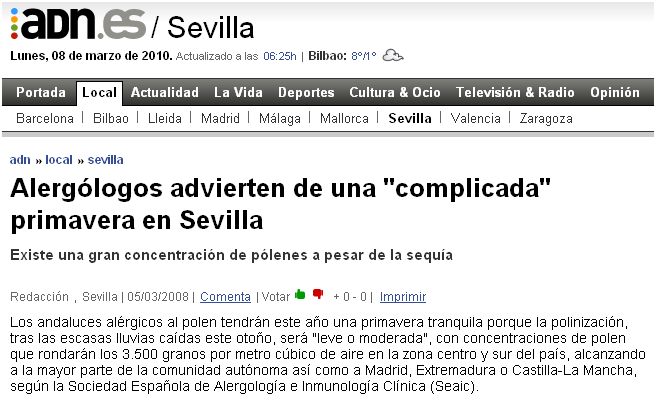
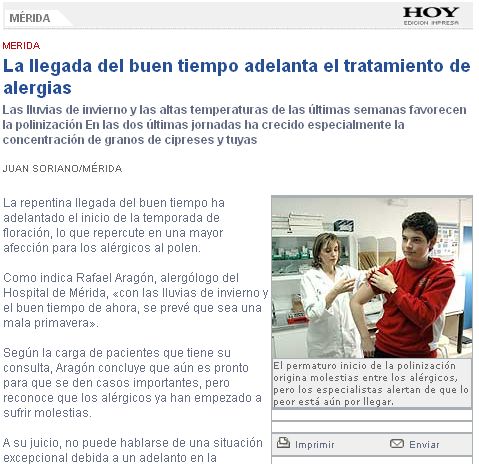
Lo que marca el cercano advenimiento de la primavera no es el olor a torrijas tempraneras, tampoco las golondrinas becquerianas, ni siquiera los anuncios de unos grandes almacenes. Desde hace unos años lo que anuncia que la estación florida se acerca sin remedio es el aviso por parte de los alergólogos de que ese año, si ese año, las alergias van ser particularmente intensas.
El problema es que todos los años son ese año o casi, véase la muestra
marzo 2009
marzo 2007
marzo 2006
—-
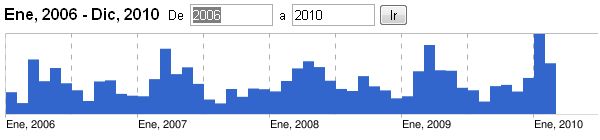
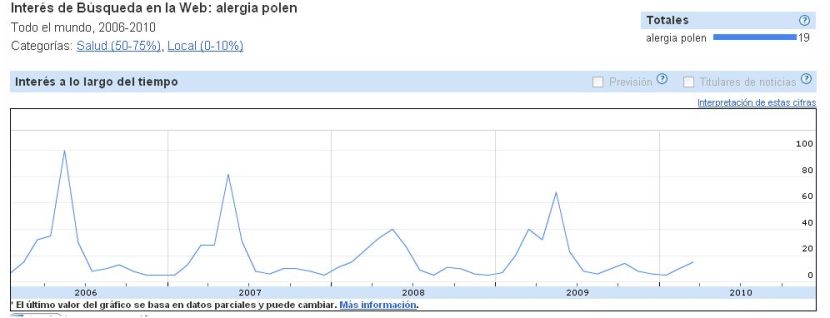
Ademas curiosamente vemos en Google que mientras la noticias sobre alergia se producen preferentemente en Marzo,
las búsquedas de los usuarios se producen en mayo
Es un ejemplo más de que la invención, exageración o promoción de enfermedades no solo procede de la malvada industria farmacéutica, surge cuasi espontáneamente cuando hay intereses de por medio. Los profesionales y las sociedades científicas no son inmunes a este pecado. Lo que sorprende es que año a año se repitan y que la prensa actué como altavoz de estos negros presagios. No importa que luego se cumplan o no, el objetivo no era alertar, sino otro ¿llenar las consultas y comenzar los tratamientos?, no lo se pero como dice un comentario de un lector del periódico 20 minutos “Para los expertos (de cualquier cosa) lo del año en curso siempre es lo peor”
otro ejemplo del sesgo del plato de lentejas y de la necesidad de acabar con los expertos
Medicina basada en la evidencia – 3
el glamour de un redescubrimiento :en la forma y manera de acceder a la información.
el triunfo de la medicina
La Dama y La Muerte un maravilloso corto español dirigido por Javier Recio, nominado a los Oscar que trata, en solo ocho impresionantes minutos, la lucha entre la muerte y los eficaces sistemas sanitarios por la vida de una anciana cansada de vivir. Gracias a El Gerente Demediado
papel bibliotecas virtuales en la investigación sanitaria
Recurso de alzada
D. ……………………., mayor de edad, con N.I.F. ………………………, y domicilio a efectos de notificaciones en ……………………………………………………………., ante la Consejería de Sanidad de la Comunidad Autónoma de Madrid comparece y, mejor proceda en Derecho, DICE:
Que mediante la presentación de este escrito y dentro del plazo legal de un mes establecido al efecto, conforme a los arts. 107, 110, 114 y 115 de la ley 30/1992, de 26 de noviembre, de Régimen Jurídico de las Administraciones Públicas y del Procedimiento Administrativo Común, formulo RECURSO DE ALZADA frente a la Resolución emitida por la Viceconsejería de Asistencia Sanitaria (16/2009) de fecha de 14 de diciembre de 2009, por la que se dictan instrucciones para mejorar la atención sanitaria integral del paciente y la continuidad del mismo en las situaciones en las que, por la naturaleza del proceso patológico, se precise tramitar la incapacidad laboral temporal, recurso al que sirven de base los siguientes,
¿se acabaron las fichitas tarugeras?
Se han publicado en el BOE Núm. 310 Viernes 25 de diciembre de 2009 S las directrices sobre estudios posautorización de tipo observacional para medicamentos de uso humano.
 El objetivo de los estudios posautorización es generar información adicional sobre los efectos de los medicamentos, así como las características relacionadas con su utilización, en las condiciones autorizadas en su ficha técnica o bien en condiciones normales de uso, con el fin de completar la información obtenida durante las fases I, II y III y contribuir a su mejor utilización. Más concretamente, los estudios posautorización pueden realizarse con alguno de los siguientes fines:
El objetivo de los estudios posautorización es generar información adicional sobre los efectos de los medicamentos, así como las características relacionadas con su utilización, en las condiciones autorizadas en su ficha técnica o bien en condiciones normales de uso, con el fin de completar la información obtenida durante las fases I, II y III y contribuir a su mejor utilización. Más concretamente, los estudios posautorización pueden realizarse con alguno de los siguientes fines:
- Determinar la efectividad de los fármacos, es decir sus efectos beneficiosos en las condiciones de la práctica clínica habitual, así como los factores modificadores de la misma, tales como el incumplimiento terapéutico, la polimedicación, la gravedad de la enfermedad, presencia de enfermedades concomitantes, grupos especiales (ancianos, niños, etc.), factores genéticos o factores relacionados con el estilo de vida.
- Identificar y cuantificar los efectos adversos del medicamento, en especial los no conocidos antes de la autorización, e identificar los posibles factores de riesgo o modificadores de efecto (características demográficas, medicación concomitante, factores genéticos, etc.). Con frecuencia, esto solo podrá estudiarse con precisión en grupos amplios de población y durante tiempos de observación prolongados.
- Obtener nueva información sobre los patrones de utilización de medicamentos (dosis, duración del tratamiento, utilización apropiada).
- Evaluar la eficiencia de los medicamentos, es decir la relación entre los resultados sanitarios y los recursos utilizados, utilizando para ello análisis farmacoeconómicos, tales como los de coste-efectividad, coste-utilidad, coste-beneficio o comparación de costes.
- Conocer los efectos de los medicamentos desde la perspectiva de los pacientes (calidad de vida, satisfacción con los tratamientos recibidos, etc.).
Pues esos son los objetivos y no otros
Feliz año
Feliz Navidad
pues eso los mejores deseos para todos y una muy Feliz Navidad
…….. y sigue habiendo un mundo fuera de nuestra ventana y demasiada gente que sigue sin saber que hoy es Navidad